1 - Introduction
Au sein de ce genre bactérien récemment découvert en constante augmentation, Helicobacter pylori est l'agent étiologique de pathologies gastro-duodénales telles gastrites chroniques et ulcères. Il joue un rôle important dans la genèse des cancers gastriques. Ceci a conduit non seulement à réviser le traitement des ulcères, mais aussi à chercher à éradiquer cette bactérie qui infecte plus de 50% de la population mondiale.
2 - Historique
| Marshall Barry et Warren Robin, médecins australiens, ont cultivé pour la première fois en 1982 Helicobacter pylori, bactérie présente à la surface de la muqueuse gastrique, car capable de survivre et de persister malgré l'acidité gastrique et la forte réponse immunitaire. Leur hypothèse est qu'elle pouvait être à l'origine de pathologies inflammatoires chroniques gastro-duodénales comme la maladie ulcéreuse. Ce n'est que plusieurs années plus tard que le bien-fondé de celle-ci fut largement accepté, ainsi en France en 1995. Prix Nobel de Physiologie ou de Médecine en 2005 |
 |
3 - Habitat- Epidémiologie
H. pylori est trouvé chez plus de 90% des personnes souffrant d'un ulcère duodénal et chez environ 80% de celles qui ont un ulcère gastrique. L'infection à H. pylori est l'une des infections chroniques les plus répandues dans le monde : de 20 à 90 % des individus adultes sont infectés selon les pays, l'infection étant plus fréquente dans les pays en développement que dans ceux industrialisés. La bactérie se transmet probablement directement d'homme à homme par voie orale. Tout se joue au stade de l'enfance : si un individu n'est pas infecté avant l'âge de 10 ans, il a très peu de risque de l'être plus tard. Elle est présente chez d'autres espèces de primates. En revanche, on ne sait pas si elle peut exister sous une forme résistante dans l'environnement, dont l'eau.
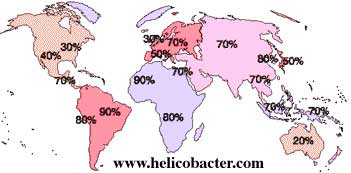 |
Les données épidémiologiques récentes ont montré qu'il existait une association entre l'infection à H. pylori et le carcinome gastrique. La proportion très limitée de sujets infectés qui développent un cancer gastrique peut s'expliquer par des facteurs environnementaux (nutritionnels), des facteurs de l'hôte (certains allèles de l'IL-1b) et des facteurs bactériens (souches cag +). Cette association ne concerne que les cancers du corps de l'estomac (dits distaux) et non les cancers du cardia (dits proximaux) représentant 20% des cas et se rapprochant des cancers de l'œsophage. http://www.helico.com/info |
4 - Pouvoir pathogène
 |
Agent étiologique des pathologies gastro-duodénales telles gastrites chroniques, ulcères gastro-duodénaux, il joue un rôle important dans la genèse des cancers gastriques. L'infection à H. pylori s'acquiert dans l'enfance. Dans la très grande majorité des cas, elle devient chronique, persiste plusieurs dizaines d'années, voire toute la vie. Chez la plupart des individus, la gastrite chronique évolue sans autre conséquence et reste asymptomatique. Environ 10% des personnes infectées développeront une maladie ulcéreuse et 1% un cancer gastrique. |
5 - Physiopathologie
|
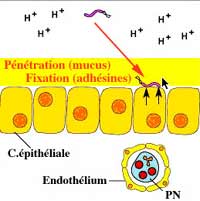
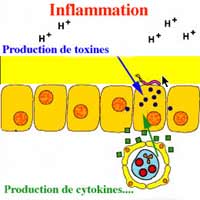
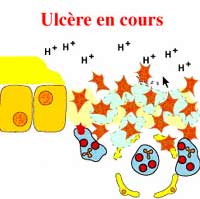
La bactérie traverse, au niveau de la muqueuse gastrique, la couche de mucus et vient se fixer sur les cellules épithéliales. Ce contact va induire des chémokines, notamment l'interleukine 8 (IL-8), attirant et activant les polynucléaires et les macrophages. Cette bactérie augmente la perméabilité de la muqueuse permettant le passage d'antigènes dont l'uréase activant également polynucléaires et macrophages. Des cytokines pro-inflammatoires (TNFa, IFN-g) sont alors libérées. L'inflammation (gastrite chronique) va persister toute la vie du sujet, sauf éradication. L'évolution de cette gastrite vers des lésions d'atrophie a été décrite avec la cascade de Correa mènant vers la métaplasie intestinale, la dysplasie et le carcinome. Au niveau de la muqueuse gastrique, H. pylori entraîne une réaction inflammatoire persistante toute la vie et considérée comme responsable de la carcinogenèse via l'apoptose, la prolifération cellulaire compensatrice des cellules gastriques et l'augmentation du risque de mutation.
Avec animation: http://www.cat.cc.md.us/courses/bio141/lecguide |
 |
 |
 |
Son génome est connu (3 souches) mais la fonction de nombreux gènes n'est pas précisée. La proportion de gènes varie d'une souche à l'autre de 20 à 30% avec l'éventuelle existence de gènes carcinogènes.
6 - Diagnostic
 |
Le Groupe d'Etudes Français des Helicobacter (GEFH) a recommandé le dépistage de H. pylori et l'éradication chez toutes les personnes infectées afin de prévenir la survenue des cancers gastriques. Des outils de diagnostic fiables et non invasifs sont disponibles. Cette recherche de la présence de H. pylori doit être systématique chez les personnes à risque élevé: - les malades ayant un ulcère prouvé - les malades ayant eu une gastrectomie partielle pour cancer - les parents du premier degré de malades ayant un cancer gastrique - les malades ayant des lésions prénéoplasiques (gastrite atrophique…) - les malades ayant un lymphome du MALT (Mucosa Associated Lymphoid Tissue), tumeur rare susceptible de régresser après traitement anti H. pylori. |
Modalités:
Les 3 méthodes actuelles sont 1: la sérologie, 2: le test respiratoire, 3: la recherche d'antigènes dans les selles (méthodes non invasives) et 4: la biopsie (méthode invasive).
| Méthodes non invasives | 1 : la sérologie |
| 2 : le test respiratoire | |
| 3 : la recherche d'antigènes dans les selles | |
| Méthode invasive | 4 : biopsies au nombre de trois |
|
. examen anatomo-pathologique
|
|
|
. test à l'urée
|
|
|
. cultures
|
|
|
. amplification génique
|
|
1 : La sérologie, méthode non invasive est utile en dépistage mais cependant réservée à des laboratoires spécialisés. Cependant, elle reste toutefois positive de nombreux mois aprés l'éradication. La technique la plus utilisée est de type ELISA. La sensibilité et la spécificité varient selon les kits commercialisés. |
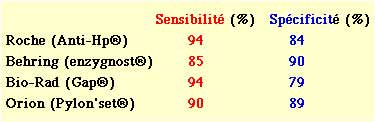 Le test PREMIER Helicobacter pylori a une sensibilité relative de 93,8 % et une spécificité relative de 95,5%. |
. Les IgM ne sont pas détectées
. Les IgG n'apparaissent que 3 semaines après le début de la maladie
. La présence d'IgA peut être parfois détectée en l'absence d'IgG.
L'autre technique, peu utilisée en dehors de laboratoires spécialisés, est dénommée immunoblotting ou western-blot. Deux kits sont commercialisés : Helico-Blot 2 ®(Genelabs Diagnostic) et Bionobis® qui permettent de préciser le diagnostic dans les « zones douteuses » de l'ELISA.


|
.Cette technique permet de définir des profils d'anticorps sériques avec : |
 |
|
Parmi les autres méthodes proposées, la recherche d'antigènes dans les selles présente un intérêt indéniable. Chez des sujets dont l'infection était prouvée par fibroscopie/biopsie, le dosage immunologique des antigènes a révélé une sensibilité de 96 %, une spécificité de 93 % et des valeurs prédictives positive de 92 % et négative de 96 %. |
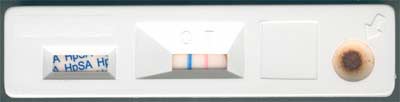 ImmunoCard STAT!HpSA ® ImmunoCard STAT!HpSA ® |
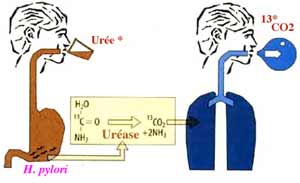
2 : Le test respiratoire ou analyse de l'air expiré consiste à faire absorber au patient de l'urée marquée au carbone 13 ou 12, puis à rechercher la présence ou l'absence de l'isotope dans le gaz carbonique expiré.
|
Si la bactérie est présente dans l'estomac, l'urée se scinde et libére le carbone 13 (ou 12) qui passe dans le sang puis les poumons et se retrouve dans l'air expiré. Ce test, fiable à plus de 98 %, présente l'avantage de rechercher la présence de la bactérie dans la totalité de l'estomac. |
 |
 |
Le dépistage par le test respiratoire à l'urée marquée (C13*) est disponible en France (Héli-Kit ®) (http://www.vidal.fr/Medicament/Heli_kit-8003.htm). Le médecin prescrit le kit que le patient achète en pharmacie (de l'ordre de 38 euros) et apporte à un laboratoire d'analyses médicales (LABM) de son choix qui effectuera le prélèvement d'air expiré dont l'analyse finale sera effectuée après envoi postal à un laboratoire spécialisé: http://www.cnrch.u-bordeaux2.fr/ . |
|
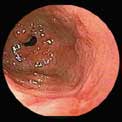
4 : La méthode invasive fait appel à des biopsies (surtout au niveau de l'antre et du fundus) lors d'une endoscopie, par exemple pour un malade qui réagit peu au traitement. Il est alors possible après culture d'effectuer un antibiogramme et de vérifier la sensibilité au traitement. |
 |
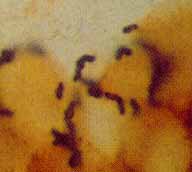
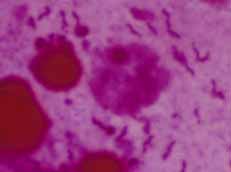
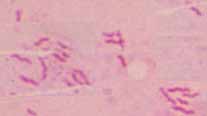
| De manière idéale, trois biopsies devraient être réalisées dont une pour un examen anatomo-pathologique. L'examen des biopsies par la coloration de Warthin Starry (à gauche) ou celle de Gram (à droite) permet de mettre en évidence des bactéries incurvés à la surface de l'épithélium de la muqueuse et parfois dans le cytoplasme des cellules. |
  |
|
. la deuxième biopsie permet la réalisation d'un test rapide à l'urée (milieu de urée-indole) par simple virage d'un indicateur de pH après incubation de 24 h à 37°C. . enfin la troisième biopsie permet la réalisation de cultures au laboratoire. |
 |
Cultures
La dernière biopsie est broyée avec du bouillon nutritif (0,3 ml) dans un appareil de Potter et ensemencée:
- sur une gélose sélective Helicobacter pylori (PYL)(bioMérieux)
- sur une gélose Columbia/Brucella/Wilkins Chalgren à 10% de sang de cheval.
|
Les boites sont placées en atmosphère microaérophile (10% de C02) et examinées après 4 jours, puis tous les 3-4 jours pendant 15 jours.
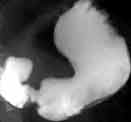
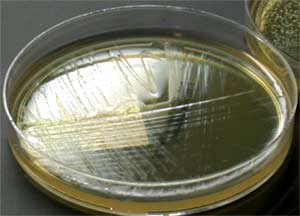
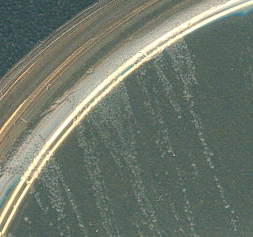
Après une incubation de 2 à 5 jours à 37° C et dans une atmosphère appauvrie en oxygène, la croissance obtenue sur une gélose chocolat ou enrichie au sang de mouton se traduit par l'apparition de colonies translucides, non pigmentées et d'un diamètre de 1 mm. |
 |
 |
 |
 |
 |
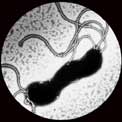
| Principaux caractères bactériologiques: H. pylori est un petit bacille (0,5 µm de diamètre sur 2 µm de longueur), à Gram négatif, légèrement incurvé, dépourvu de fibre périplasmique, mobile grâce à de multiples flagelles entourés d'une gaine et disposés selon une ciliature péritriche. |
 |
|
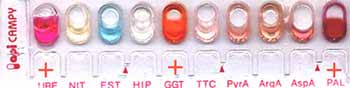
C'est une bactérie micro-aérophile (mais capable de croître en anaérobiose en présence de C02), catalase +, oxydase +, nitrate réductase +, uréase ++++, n'acidifiant pas les sucres, cultivant à 30° et à 37°C. |
 |
Les souches peuvent être adressées au Centre National de Référence (CNR) à l'adresse suivante: http://www.cnrch.u-bordeaux2.fr/

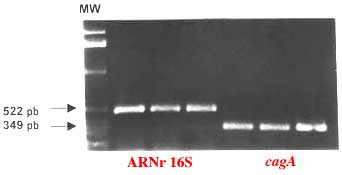 |
Les méthodes moléculaires telles amplification génique (PCR) suivie ou non d'un séquençage sont peu utilisées dans la recherche directe ou après culture. L'amplification des gènes codant pour les ARNr 16S (suivie du séquençage des amplicons) ou encore du gène cagA est possible pour confirmer rapidement le diagnostic. La PCR de l'ARNr 23S permet de diagnostiquer la résistance acquise aux macrolides (clarithromycine). |
7 - Traitement - Sensibilité aux antibiotiques
- En France, le traitement est actuellement recommandé chez les malades ayant un ulcère prouvé ainsi que chez ceux ayant un lymphome du MALT ou encore l'entourage d'un nouveau malade identifié, voire lors d'atrophie gastrique identifié simplement par recherche d'antigène dans les selles.
(http://www.pasteur.fr/actu/presse/com/communiques/03Helicobacter.htm).
- Celui-ci est une trithérapie de 7 jours associant un inhibiteur puissant de l'acidité gastrique (inhibiteur de la pompe à protons à double dose) et deux antibiotiques, le plus souvent l'amoxicilline et la clarithromycine (macrolide) ou encore le métronidazole, si possible guidé par l'antibiogramme.
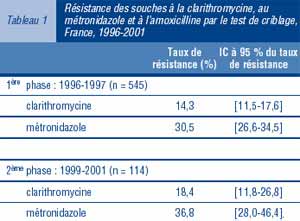
- La bactérie est éradiquée dans plus de 70 % des cas après un premier traitement. Les facteurs d'échec sont : résistance à la clarithromycine retrouvée dans 12 à 14 % des cas, mauvaise observance du traitement, âge < 50 ans et tabagisme.
- Après un traitement de deuxième ligne, 90 % des patients sont guéris de leur infection.
- Antibiogramme : La notion de résistance acquise aux antibiotiques de type macrolide ou imidazole amène à la rechercher pour des raisons épidémiologiques lors d'isolement d'une souche par une technique récemment standardisée de l'antibiogramme (CA-SFM 2004)(http://www.sfm.asso.fr/nouv/general.php?pa=2, page 5).
* Gélose : Mueller-Hinton (Oxoïd) supplémenté avec 10% sang de cheval
* Inoculum : 3 unités MacFarland en sérum physiologique
* Antibiotique à tester: érythromycine (E)
* Méthodes: Diffusion, dilution ou E-test
Erythromycine: Diamètres critiques provisoires: > 22 et < 17 mm et concentrations critiques: < 1 et > 4 mg/l.
Exemple d'antibiogramme pour les macrolides dont l'érythromycine (E)

*H. pylori est sensible à l'amoxicilline (CMI = 0,12 mg/l). Cette activité est améliorée d'un facteur de 10 à 20 par un pH variant de 5,5 à 7,5. Il n'a pas été décrit de résistance acquise. La posologie recommandée est de 2 g/jour en deux prises. La concentration critique pour la résistance acquise est > 0,5 mg/l.
* La clarithromycine est le seul macrolide réellement évalué, avec une bonne diffusion tissulaire. Les posologies efficaces sont de 250 mg x 2/jour et 500 mg x 2/jour. La résistance primaire (CMI > 1 mg/l) atteint déjà en France 10 à 20% des souches isolées (cf http://www.invs.sante.fr/publications/).
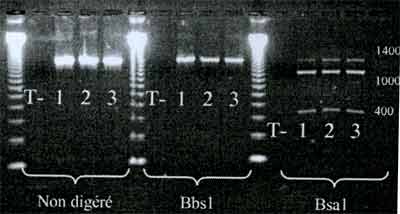
La résistance peut être détectée par PCR de l'ARNr 23S suivie d'une digestion-restriction (BSA1 et Bbs1).
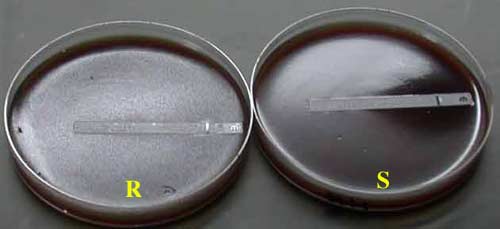
* Les nitroimidazolés sont aussi actifs, car sécrétés activement au niveau de la muqueuse avec des concentrations élevées dans le mucus. Leur activité est peu influencée par les modifications de pH. La résistance de H. pylori est malheureusement élevée > 30% en France (concentration critique > 8 mg/l). La posologie est de 1 g/jour en deux prises tels métronidazole et tinidazole.
Détection de la résistance par E-test
8 - Prophylaxie
L'incidence élevée de cette infection dans la population et les conséquences qu'elle implique, notamment le risque de développer un cancer de l'estomac, justifient la recherche soit d'un vaccin contre cette bactérie soit de nouvelles molécules capables de l'éradiquer tels les gènes de l'uréase dont les deux sous-unités, UreA et UreB administrées à des souris, ont permis de protéger 70% d'entre elles contre l'infection.
L'infection à Helicobacter n'est pas une infection à déclaration obligatoire. Elle fait l'objet actuellement d'une surveillance par l'Institut de Vieille Sanitaire (INVS)(Surveillance nationale des maladies infectieuses, 1998-2000, http://www.invs.sante.fr/publications/index.html#mi).
Ce cours a été préparé avec la collaboration du Docteur J. Raymond (Groupe hospitalier Cochin-Saint-Vincent de Paul, Faculté de Médecine Cochin-Port-Royal, Université Paris V)(Version 2, 06.02.04).
|
|
|
|
|