1 - Introduction
Dans toutes les familles de virus à ADN on peut trouver des virus capables de ‘transformer’ des cellules hôtes : l'infection par ces virus entraîne une modification génétique définitive de la cellule qui devient cancéreuse et prolifère de façon incontrôlée.
Il n'existe qu'une seule famille de virus à ARN dans laquelle on trouve des virus oncogènes (oncogène : (onco = masse – qui engendre une masse).
Désigne couramment tout gène impliqué dans la genèse d’un cancer ou caractérise un virus capable de cancériser) : ces virus ont été appelés virus oncogènes à ARN ou Oncornavirus (Onco – RNA – virus).
On s'est longtemps demandé comment un génome viral ARN pouvait transférer définitivement une information génétique ADN dans un génome cellulaire.
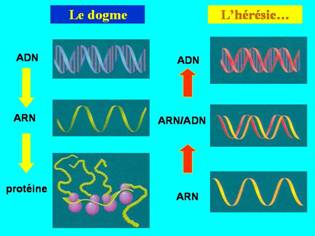
Comme l’ont démontré Howard Temin et David Baltimore, c'est parce que les Oncornavirus possèdent une enzyme qui rétrotranscrit l'ARN viral en ADN bicaténaire ; l'enzyme peut inverser le sens de transmission de l'information génétique, sens qui avait été établi comme le "dogme" de la biologie moléculaire :
le "dogme" : (ADN)2 ARN protéine
les Oncornavirus : (ADN)2 ARN
En transportant et en intégrant la réplique d’un oncogène dans un chromosome, le virus peut effectivement modifier définitivement l'information génétique de la cellule hôte.
L'enzyme, isolée en 1978, est appelée la transcriptase inverse ou rétrotranscriptase, et les virus à ARN possédant cette enzyme sont appelés des Rétrovirus.

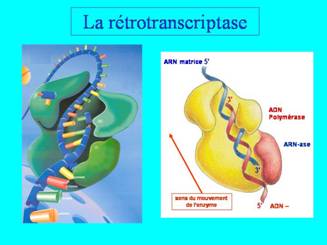
Cet ADN bicaténaire viral est appelé un provirus : il est désormais équivalent à un gène cellulaire et pourra, dans certaines conditions, être transcrit par la machinerie cellulaire. Les ARN viraux produits sont cappés et poly-adénylés. Ils peuvent être soumis ou non à épissage.
Classification des Retroviridae (Rétrovirus)
Sur la base de critères de pathogénicité on distingue trois sous-familles :
1° - Les Oncovirinae (Oncovirus) :
ce sont des virus transformants.
La sous-famille des Oncovirinae est la plus importante des trois. On a trouvé des oncovirus chez les insectes, les sangsues, les reptiles, les oiseaux et les mammifères.
Les Oncovirus peuvent induire les tumeurs les plus variées :
bien connus chez les oiseaux et rongeurs, ils sont associés au développement de sarcomes (tumeurs du tissu conjonctif), de carcinomes (tumeurs des tissus épithéliaux), de lymphomes et de leucémies. C'est ce dernier type de tumeur qui est le plus fréquent dans la pathologie rétrovirale.
En 1980, Robert Gallo a isolé le premier rétrovirus humain. Celui-ci est impliqué dans le développement d'une leucémie à lymphocytes T : le virus HTLV-1 (pour human T cell leukemia virus). Il a ensuite isolé un second virus, le virus HTLV-2, sans qu'une pathologie puisse encore lui être attribuée avec certitude.
HTLV-1 : répartition géographique et structure
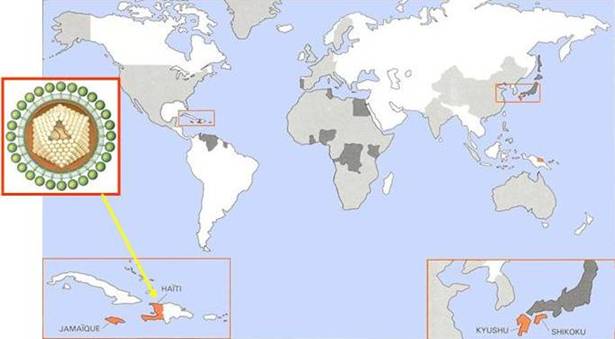

2° - Les Spumavirinae (Spumavirus) :
ce sont des virus "non pathogènes"
Ces virus ont été découverts par hasard au début des années 1950 chez plusieurs espèces animales : singes, bovins, chats, hamsters. où ils provoquent des infections inapparentes. On les a également isolés chez l'homme (1970).
Les cellules infectées in vitro présentent des lésions qui ressemblent à de l'écume (spuma = mousse).
3° - Les Lentivirinae (Lentivirus) :
ce sont des virus cytopathogènes
Ces virus ont d'abord été isolés chez l'animal et sont responsables de maladies à évolution lente (lentus = lent).
Les virus de l'immunodéficience humaine VIH-1 et VIH-2appartiennent à cette sous-famille.
|
Le VIH donne une infection chronique, caractérisée par une phase de latence clinique très longue ,pouvant atteindre dix ans. |
S VIRUS DE L’IMMUNODEFICIENCE HUMAINE
I – DECOUVERTE DES VIRUS DE L’IMMUNODEFICIENCE HUMAINE
LE VIH-1
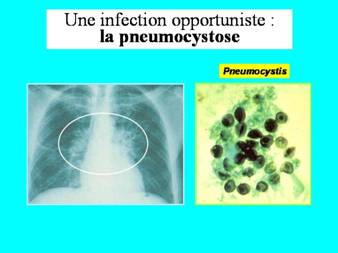
En juin 1981, le CDC d'Atlanta (Center for Disease Control), qui centralise les informations sur la situation des maladies infectieuses, annonce, dans son Bulletin hebdomadaire, que des médecins de Los Angeles, San Francisco et New York ont signalé l'accroissement récent du nombre de cas de pneumonies à Pneumocystis carinii (un champignon) et de sarcomes de Kaposi, les deux affections étant parfois associées.
La pneumonie à Pneumocystis carinii (la pneumocystose), affection rarissime jusqu'alors, était connue comme une infection opportuniste touchant presque exclusivement les sujets en état d'immunodépression profonde.
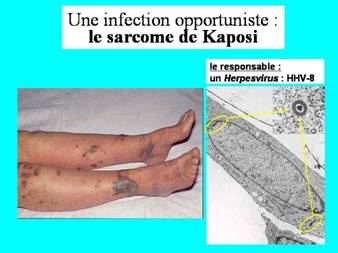
Le sarcome de Kaposi, quant à lui, est très rare, ne touchant que les hommes âgés ou des sujets transplantés qui reçoivent une thérapeutique immunosuppressive.
Or, tous les cas recensés par les médecins correspondaient à des hommes jeunes, précédemment en bonne santé et tous homosexuels. On parle alors du "Gay syndrome"…

Puis, dans les mois qui suivent, d'autres groupes vont se joindre à celui des homosexuels : les toxicomanes par injections intraveineuses d'héroïne, les Haïtiens et enfin les hémophiles... L'ensemble des malades va constituer le "groupe des quatre H"...
Homosexuels Héroïnomanes Haïtiens Hémophiles
Les examens de laboratoire révèlent chez tous ces malades un effondrement de l'immunité cellulaire :
- anergie des tests cutanés à certains antigènes courants (tuberculine...)
- lymphopénie inférieure à 500/mm3
- diminution des lymphocytes T helpers (T CD4+)
d'où le nom donné au syndrome :
syndrome d'immunodéficience acquise ou Sida.
Mais quel est l'agent responsable du syndrome ?
La transmission du sida par la voie sexuelle (chez les homosexuels et les haïtiens), par la voie sanguine (chez les héroïnomanes et les hémophiles) est analogue à la transmission de l'hépatite B et rend très probable l'origine virale de la maladie.
On incrimine tout d'abord divers virus fréquemment détectés chez les sujets atteints de Sida : le cytomégalovirus (CMV), le virus d'Epstein-Barr (EBV), le virus de l'hépatite B (HBV).
Mais tous ces virus sont en fait responsables d'infections opportunistes qui sont la conséquence et non la cause de l'immunodéficience.
· Robert Gallo, qui a découvert en 1980 le premier rétrovirus humain, considère le HTLV-1 comme la cause probable du Sida.
· Luc Montagnier, spécialiste des Oncornavirus (Institut Pasteur de Paris), cherche à mettre en évidence la rétrotranscriptase dans une culture de cellules infectées :
En janvier 1983, un ganglion cervical est excisé à l'hôpital de la Pitié (Paris) chez un homme de 33 ans, qui présente des troubles mineurs mais suffisants pour suspecter le Sida (la lymphadénopathie est un symptôme précoce du Sida). Ce patient homosexuel, steward d'une compagnie aérienne, avait séjourné à New York en 1979 et avait des relations avec plus de 50 partenaires par an.
Les lymphocytes sont mis en culture avec de l'IL-2. Au quinzième jour, une activité rétrotranscriptase est détectée. Mais la culture s'épuise. Le virus est alors propagé à une culture de lymphocytes T de sujet sain. L'activité de l'enzyme est retrouvée, elle augmente, puis diminue.
Le virus isolé ne peut pas être le virus HTLV-1 :
· en culture, HTLV-1 augmente la prolifération des lymphocytes T et de ce fait, la production de rétrotranscriptase. Le virus hypothétique se comporte différemment : il n'active pas les lymphocytes T, il les tue.
· le virus est identifié en microscopie électronique, il ne ressemble pas au HTLV-1.
Montagnier informe Gallo de ses résultats. Ce dernier lui envoie des anticorps anti-HTLV qui ne réagissent pas avec le rétrovirus isolé.
Ce premier nouveau rétrovirus ("français") provenait d'un malade sans Sida avéré. Montagnier démontre la présence de ce même virus chez les malades affectés des formes les plus diverses du Sida.
L'équipe française prouve que le virus attaque les lymphocytes T4 ;au lieu de les immortaliser comme le fait le virus HTLV, il les détruit. Ce virus ne peut pas être un Oncovirus mais plutôt un Lentivirus.
Après sa découverte, le virus a porté des noms divers. En 1986, il est inscrit à la nomenclature internationale sous l’appellation de HIV pour Human Immunodeficiency Virus. En France, il a rapidement été rebaptisé VIH.
Le patient Bru..., porteur de la souche initiale du VIH est resté quelques années sans symptômes majeurs. La maladie a néanmoins fini par se manifester et, en automne 1988, il est mort du Sida.
Le VIH-1 a une diffusion mondiale.
Le VIH 2
Le VIH-2 a été isolé par l’équipe de Montagnier en 1985 chez des sujets portugais atteints de Sida (contracté dans les colonies portugaises de l'Afrique de l'Ouest), mais dont la sérologie VIH-1 restait négative.
Antigéniquement distinct de VIH-1, le VIH-2 est moins pathogène.
La diffusion du VIH-2 demeure actuellement restreinte à l'Afrique de l'Ouest.
II - STRUCTURE DES VIRUS DE L'IMMUNODÉFICIENCE HUMAINE
1 - Morphologie
Morphologie et structure des virus VIH-1 et 2 sont sensiblement identiques.
Les particules virales mûres sont grossièrement sphériques. La capside a une forme en tronc de cône.
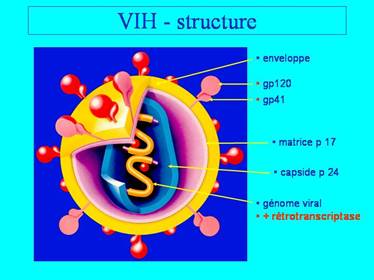
On distingue :
- une enveloppe :
· dans laquelle sont incluses des spicules formées par l'association de molécules de glycoprotéine virale structurée en deux sous-unités :
- la gp120 : qui se fixe au récepteur cellulaire.
(SU gp120 : SU pour surface) gp120 : gp = glycoprotéin 120 = PM de 120 kilodaltons
- la gp41, liée à la gp120, est responsable de la fusion de l'enveloppe avec la membrane cellulaire.
(TM gp41 : TM pour transmembranaire)
· la protéine MA (MA pour matrice) tapisse la face interne de l'enveloppe et constitue la matrice.
- une capside :
En forme de tronc de cône, la capside est formée par l'assemblage de la protéine CA p24 (CA pour capside, p pour protéine).
La capside contient le génome viral et un complexe enzymatique:
le génome
· 2 molécules d’ARN (>+) monocaténaires identiques d'environ 9,7 kb sont présentes dans la capside. Bien que de polarité positive, ces ARN ne sont pas utilisés directement comme ARN messagers.
· les deux ARN sont étroitement associés à des protéines NC (pour nucléocapside), qui les réunissent et les protègent de l'activité des enzymes cellulaires.
des enzymes : la rétrotranscriptase, l'intégrase, une protéase. On trouve dans chaque virion une cinquantaine de molécules de chaque enzyme.
La rétrotranscription est déjà engagée dans les capsides matures, à partir d’une amorce embarquée et constituée par un ARN-t cellulaire
2- Analyse du génome des Rétrovirus
Le génome code les protéines virales. Il est encadré par 2 régions non codantes appelées LTR (Long Terminal Repeats). De 5' en 3' on trouve :
Le LTR5'
le gène gag (pour group specific antigens) code une polyprotéine qui sera découpée en protéines (de capside, de nucléocapside et de matrice) par la protéase virale,
le gène pol (pour polymérase) code les trois enzymes : la rétrotranscriptase, l'intégrase et la protéase,
le gène env (pour enveloppe) code une protéine précurseur qui sera glycosylée (la gp160) puis clivée en TM gp41 et SU gp120 qui, restant associées, vont constituer les spicules, en s’oligomérisant.
Par découpage du génome viral, on trouve également chez les Lentivirus de petits gènes de régulation.
Le LTR3'
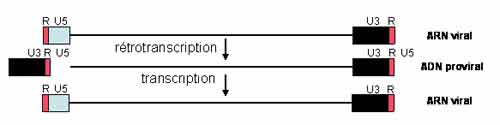
Les 2 LTRs ne sont complets (U3 R U5) qu’au niveau du provirus
3- Analyse des LTRs (régions non codantes) des ARN génomiques
Ce sont les régions stratégiques du virus. On y trouve des signaux de régulation de la transcription (en ARN) et de la traduction (en protéines), des séquences d'amorçage de la réplication, des signaux pour l'intégration et pour l'encapsidation (les régions non codantes 5' et 3' sont agrandies environ dix fois ) :
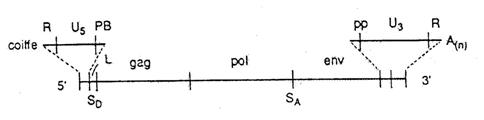
La région non codante 5'
|
coiffe |
l'extrémité 5' comporte tout d'abord une coiffe, comme un ARN-m. |
|
R |
elle est longue d'une centaine de nucléotides. (R pour Repeat car cette région R est répétée dans la région non codante 3'). |
|
U5 |
(U5, pour Unique en 5'), longue d'une centaine de nucléotides. |
|
PB |
(PB, pour primer binding site), longue de 18 nucléotides. (primer = amorçe) ce site fixe un ARN-t cellulaire. |
|
L |
(L, pour Leader). |
|
SD |
(SD pour site donneur) : site servant à l'épissage des ARN-messagers. |
| SA |
entre les gènes pol et env, SA est le site accepteur d'épissage des ARN-m. |
La région non codante 3'
|
pp |
(pp pour poly-purine), séquence de 1 à 20 nucléotides riche en purines, reconnue par la rétrotranscriptase. |
|
U3 |
(U3, pour Unique en 3'), longue d'environ 500 nucléotides. |
|
R |
(R pour repeat) séquence identique à la séquence R en 5'. |
|
A (n) |
100 à 200 nucléotides à Adénine (c'est la queue poly A caractéristique des ARN-m). |
III – LA MULTIPLICATION DU VIRUS
1° du virus (ARN) au provirus (ADN)
Le virus se fixe sur la cellule en se liant au récepteur CD4 puis à un corécepteur, CXCR4 pour le lymphocyte, CCR5 pour le macrophage. Il peut alors pénétrer par la voie classique de l’endocytose qui aboutira à sa destruction dans le lysosome. En fait, son entrée infectante efficace est réalisée par fusion directe de son enveloppe avec la membrane plasmique de la cellule cible.
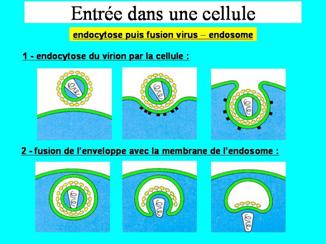
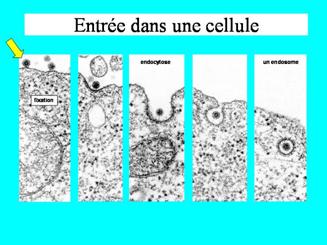
Action des corécepteurs et fusion des membranes
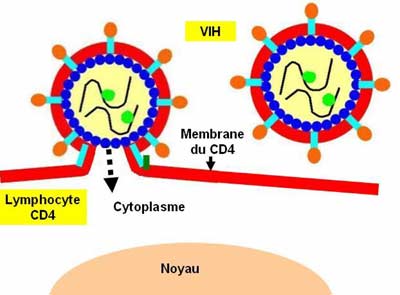
- fixation par gp 120
La gp120 se fixe au récepteur cellulaire CD4.
· la molécule CD4 caractérise les lymphocytes T-auxiliaires (les lymphocytes Th ou CD4+).
· elle est également présente sur les macrophages, les cellules dendritiques des ganglions, de la rate et de l'épiderme (les cellules de Langerhans) ainsi que sur les cellules microgliales du cerveau (qui sont les macrophages résidents du SNC).
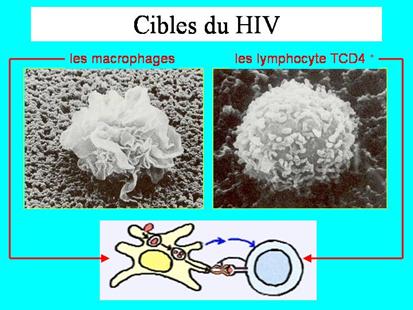
- sur les lymphocytes Th (T) : CXCR4
La région de gp 120 qui se fixe au co-récepteur s'appelle la boucle V3 (V pour variable) :
· une infection VIH par voie muqueuse s'établit avec une souche à tropisme M
· puis des variants vont apparaître au cours de l'infection, dotés d'un double tropisme M et T
· en phase terminale de la plupart des infections, la majorité des virus ont un tropisme T
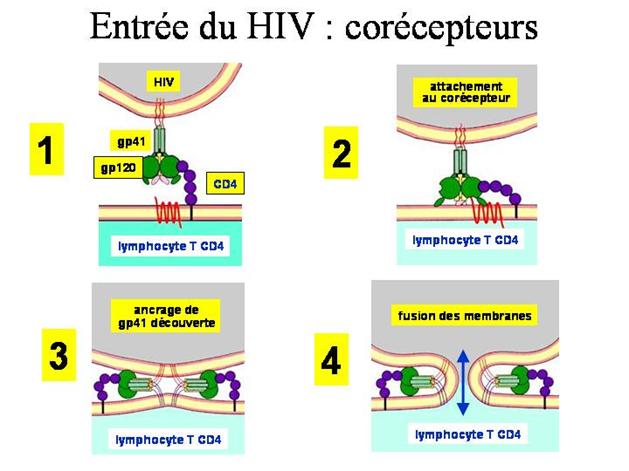
- pénétration par fusion
Après s'être fixée à CD4, gp120 doit trouver un second récepteur cellulaire, un co-récepteur :
il se forme un complexe trimérique CD4 - gp 120 - co-récepteur indispensable pour permettre à la glycoprotéine gp 41 d'exercer son activité fusionnante.
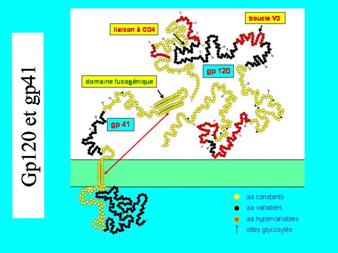
- décapsidation
dans le cytoplasme, la capside se désagrège et libère le génome.
- réplication
dans le cytoplasme de la cellule hôte, la rétrotranscriptase virale :
1°- copie l'ARN en ADN simple brin,
2°- hydrolyse le brin d'ARN,
3°- copie l'ADN simple brin pour former un ADN bicaténaire.
La réplication suit un mécanisme très complexe qui conduit à la création de séquences particulières aux extrémités de l'ADN proviral : les LTR (long terminal repeat), nécessitant en particulier un ‘saut de brin’ de la rétrotranscriptase entre les 2 molécules d’ARN viral amenées par la capside virale
Bien que ces séquences soient identiques, elles ne vont pas jouer le même rôle :
· en 5' le LTR est un promoteur puissant de la transcription,
· en 3' le LTR fournit le signal de coupure qui précède la polyadénylation. C'est aussi un promoteur potentiellement capable d'activer un gène cellulaire situé à proximité.
- circularisation
l'ADN viral est transporté dans le noyau, avec l'intégrase virale, qui se fixe au niveau des LTR, et se circularise.
- intégration
l'intégrase coupe les deux brins de l'ADN cellulaire pour introduire l'ADN viral. L'intégration semble pouvoir se faire en plusieurs exemplaires dans différentes régions de l'ADN cellulaire.
l'intégration dépend aussi de l'activation des cellules infectées :
La rétrotranscription est lente et incomplète dans les cellules au repos : il se forme un ADN incomplet qui pourra être éventuellement complété si l'activation de la cellule ne survient pas trop tardivement. Sinon, l'infection avortera.
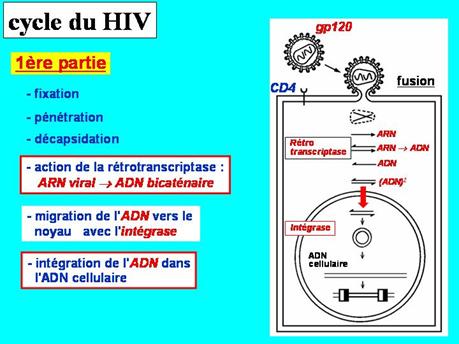
2° du provirus aux nouveaux virions
- Les 6 petits gènes de régulation
Outre les gènes gag, pol et env, le provirus des VIH-1 et 2 possède l’information pour six gènes codant de petites protéines régulatrices. Ce sont les gènes tat, rev, nef, vif, vpr, et vpu (VIH-1)ou vpx (VIH-2) :
|
tat |
(transactivator of transcription) la protéine Tat est un activateur puissant de la transcription en ARN-m et en ARN viral : en sa présence, les cellules infectées produisent 1000 fois plus d'ARN viraux. |
|
rev |
regulation of expression of viral proteins la protéine Rev permet l'exportationdes ARN viraux génomiques. Elle intervient en phase secondaire de la réplication en permettant aux ARN viraux d’échapper à l’épissage. . |
|
nef |
Regulatory factor : favorise la réplication virale et intervient dans la régulation négative de l’expression du récepteur CD4, ce qui facilite l’extériosisation des virions néoformés. |
|
vif |
virion infectivity factor la protéine Vif augmente l'infectivité des nouveaux virions formés par la cellule. |
|
vpr |
viral protein r : activateur de la transcription |
|
vpu (VIH-1) ou vpv (VIH-2) |
viral protein u rôle encore incertain dans l'assemblage des virions viral protein x |
Les séquences codantes des gènes tat et rev sont constituées par deux exons éloignés l'un de l'autre.
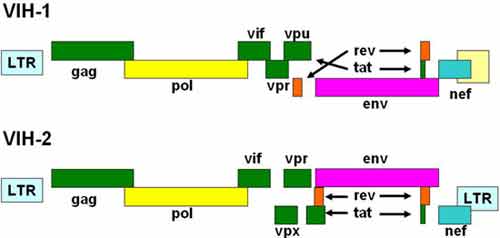
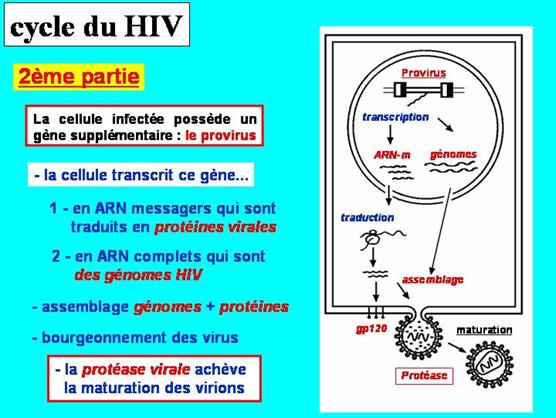
- transcription et réplication
Le provirus dépend de l'ARN polymérase cellulaire pour sa transcription
La régulation de l'expression des gènes viraux dépend à la fois de l'activité des protéines régulatrices virales et de la coopération de facteurs cellulaires.
Au début de l'expression du provirus, les gènes de régulation (épissés) sont les seuls à être exprimés. Les protéines virales régulatrices et des facteurs cellulaires activent la transcription du provirus et le transport des ARN génomiques non épissés vers le cytoplasme, permettant ainsi l’expression des gènes codant les protéines de structure et les enzymes,. Finalement, les ARN génomiques eux-mêmes pourront être encapsidés.
En résumé, le transcrit primaire d'ARN peut servir :
- d'ARN-m épissé, pour être traduit en protéines de régulation et glycoprotéine d’enveloppe.
- d’ARN-m non-épissé pour être traduit en protéines de structure et enzymatiques
- d'ARN-mnon-épissé infectieux, encapsidé.
Montage des ARN-m par excision-épissage
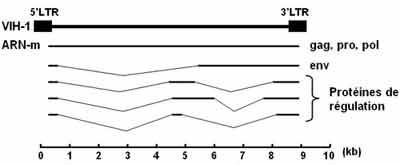
l'ARN-m d'enveloppe est excisé-épissé une seule fois, les ARN-m de régulation le sont plusieurs fois
- les 3 gènes gag, pol et env
- le transcrit primaire non épissé permet la synthèse des protéines de capside ainsi que les enzymes, nécessaires à la réplication du virus, qui seront intégrées dans les virions.
La traduction par les ribosomes génère deux polyprotéines : une polyprotéine Gag Pr p55 (90 %) - (Pr = précurseur)
- et une polyprotéine Pol Pr p180 (10 %).
Un seul ARN-m génère deux polyprotéines
En 3' du gène gag se trouve un codon stop qui est, dans 90 % des cas, interprété correctement par le ribosome et dicte, à ce niveau, l’arrêt de la synthèse de la polyprotéine Gag.
L'environnement du codon stop permet, dans 10 % des cas, un décalage du cadre de lecture et la synthèse de la polyprotéine Pol en quantité nettement inférieure à celle de la polyprotéine Gag.
Les polyprotéines migrent vers la membrane cytoplasmique où elles seront découpées en protéines internes et en enzymes sous l'action de la protéase virale.
Ce découpage survient au cours de la maturation qui s'achève après libération des particules virales.
- le transcrit primaire qui sera traduit en glycoprotéine virale ne subit qu’une seule opération d’excision-épissage.
Cette glycoprotéine d’enveloppe possède un peptide signal permettant sa fixation au réticulum rugueux et ainsi son orientation vers l’appareil de Golgi où elle subira une forte glycosylation pour donner la glycoprotéine précurseur Pr gp160 qui sera découpée en gp120 et gp41 par une protéase cellulaire :
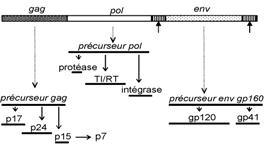
Génome et protéines du VIH-1
- encapsidation, morphogenèse et libération
Sous la membrane de la cellule, remaniée par l'insertion des glycoprotéines virales, toutes les protéines de structure s'accumulent et un dimère d'ARN s'en recouvre. L'ARN-t cellulaire est fixé sur le site convenable (PB) grâce à la protéine p15.
Les nouveaux virions bourgeonnent.
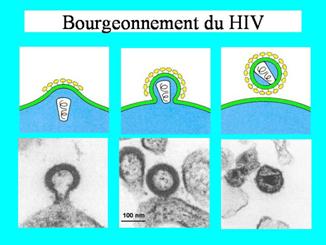
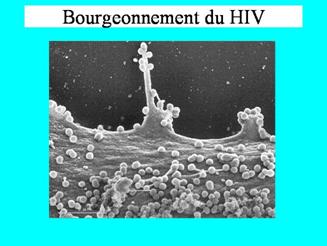
Ces particules virales sont encore immatures : la maturation des précurseurs s'achève grâce à l'activité de la protéase virale.
Application thérapeutique : un inhibiteur spécifique de la protéase virale empêche la formation de virions infectieux
- les cellules-cibles du virus
Les cellules-cibles sont essentiellement celles qui expriment à leur surface la protéine CD4 qui est le récepteur du virus. Ce sont surtout des cellules du système immunitaire : les lymphocytes T-auxiliaires et les macrophages.
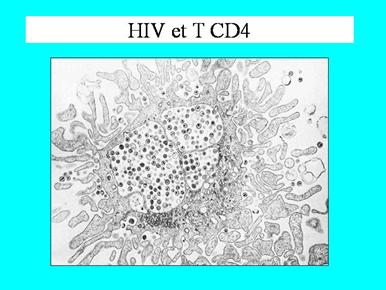
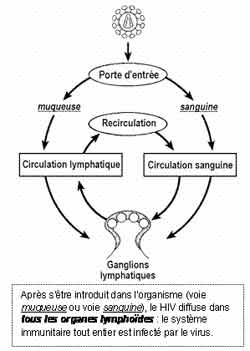
Toutes ces cellules sont principalement concentrées dans les organes lymphoïdes, en particulier les ganglions. C'est donc dans ces organes que le VIH se multiplie.
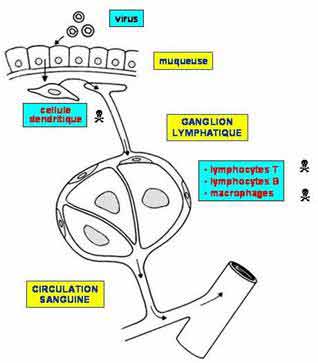
Rappels
Comme toutes les cellules du sang, les lymphocytes et les macrophages proviennent de la moelle osseuse.
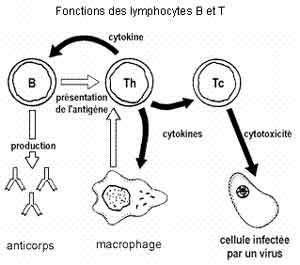
On distingue deux classes de lymphocytes : certains se différencient dans la moelle osseuse en lymphocytes B qui produiront des anticorps ; d'autres migrent vers le thymus où ils se différencient en lymphocytes T (T pour Thymus) dont on peut distinguer deux populations d'après la présence de protéines ancrées dans leurs membranes cytoplasmiques :
les lymphocytes T- auxiliaires (T- helpers ou Th)
sont caractérisés par la présence de la protéine CD4 (ce sont des lymphocytes TCD4+ ou T4).
Sans lymphocyte Th, toute réponse immunitaire à un antigène (bactérie, virus, parasite) est déficiente, d'où leur appellation de lymphocytes T auxiliaires.
Sans lymphocytes Th, on observe donc une immunodéficience.
les lymphocytes T- cytotoxiques (Tc)
sont caractérisés par la présence de la protéine CD8 (ce sont des lymphocytes TCD8+ ou T8).
Ils reconnaissent spécifiquement les cellules infectées qui expriment à leur surface la glycoprotéine virale et les détruisent, d'où leur appellation de lymphocytes T cytotoxiques.
Réponse immunitaire de l'organisme au VIH :
humorale :
avec l'apparition d'anticorps anti-VIH. Parmi ces anticorps, les anticorps anti-gp 120 se fixent aux spicules et empêchent la fixation des particules virales aux cellules-cibles.
cellulaire :
avec l'apparition de lymphocytes T-cytotoxiques qui reconnaissent les cellules qui expriment la glycoprotéine virale (en particulier les lymphocytes Th) et les détruisent
Mais comme les Th sont indispensables à l'activation des Tc, leur destruction affaiblit progressivement l'efficacité de la réponse immunitaire.
Si les Th diminuent, la réponse immunitaire globale de l'organisme diminue également,
tant vis-à-vis du VIH que des autres agents infectieux (bactéries, virus et parasites).
3° caractéristiques de la multiplication des VIH
Le changement dans la continuité… Au cours de leur multiplication, comme tous les génomes, celui des virus:
· doit assurer l’intégrité des informations indispensables à leur structure et à leurs activités enzymatiques propres.
· un nombre important de mutations est toutefois compatible avec le maintien de la réplication virale. Ces mutations resteront neutres ou permettront au virus d’évoluer dans son tropisme, sa capacité à répliquer et à échapper à certaines contraintes extérieures telles que, par exemple, les traitements anti-viraux. Dans ce cas, la pression de sélection exercée provoquera l’émergence de populations virales porteuses de mutations capables précisément de leur conférer la résistance à ces molécules.
La production de la diversité virale se faisant au hasard, elle suppose le "gaspillage" des nombreux virus qui ont subi les variations, neutres ou létales. Mais ce gaspillage est dérisoire au vu de la vitesse de multiplication virale : un virus moyennement rapide peut produire près de 10.000 virus fils par jour. Si un seul virus est présent le premier jour, il y en aura 10.000 le second, puis 10.000 fois 10.000, soit cent millions le troisième, 10.000 fois 10.000 fois 10.000, soit mille milliards le quatrième jour, etc…
La variation prend naissance au niveau des gènes
Cette variation est due aux erreurs qui surviennent lors de la réplication du génome : chaque erreur, ou mutation1, correspond à un changement de base qui ne respecte pas la complémentarité A-T, G-C.
Dans le cas du VIH, la rétrotranscriptase ne "relit" aucune des copies qu'elle exécute (ARN ® ADN) et (ADN ® ADN) et commet en moyenne une erreur sur 104 nucléotides qu'elle assemble : le génome du VIH comprenant environ 10.000 nucléotides, il existe en moyenne une différence entre deux virus frères.
Mais la sélection contrôle la tendance au changement, en éliminant les génomes non fonctionnels et en favorisant l’émergence des mutants plus aptes à la multiplication ou résistants à de nouvelles conditions extérieures :
· une mutation défavorable supprime par exemple l'activité d'une enzyme nécessaire à la multiplication du virus : le mutant qui la porte disparaît, n'ayant pas la possibilité de se reproduire.
· une mutation favorable est, par exemple, celle qui donnera au virus une glycoprotéine d'enveloppe différente puisque le mutant qui la porte peut ainsi échapper aux produits élaborés par le système immunitaire (anticorps et lymphocytes T cytotoxiques).
La conservation de mutations sans incidence sur le comportement viral aboutit à la production d’une Les populations hétérogènes sont appelées quasi-espèces.
La variabilité de la glycoprotéine gp 120L'analyse comparative des gènes de glycoprotéine gp 120 (Env) provenant de nombreuses souches de virus a permis de définir des régions constantes (C) et des régions variables (V). Le gène env a été modifié par les erreurs commises par la rétrotranscriptase et les protéines correspondantes présentent de légères différences entre elles.
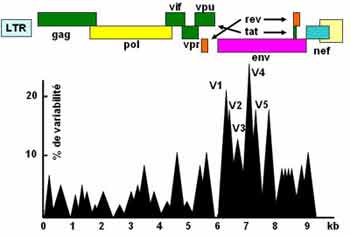
Les variations des glycoprotéines gp120 et gp41
(le graphique indique les régions variables)
Les régions constantes sont conservées car elles sont essentielles à l’infectiosité du virus :, lorsque le site de liaison de la gp 120 à la molécule CD4 est modifié, le virus ne peut plus se fixer aux cellules-cibles et disparaît, puisqu'il a perdu tout pouvoir infectieux : il a subi une mutation létale.
Les variations de séquence de la boucle V3 de la de la gp 120, (qui porte le déterminant antigénique majeur de la réponse immunitaire), ont permis de définir 9 sous-types (A B C D F G H J K), rassemblés dans un groupe M (pour Major)..
En 1989, on a isolé au Cameroun des VIH-1 dont la gp 120 ne présentait qu'une homologie très faible avec les sous-types connus : ils ont été classés dans le nouveau groupe O (pour outlier). Les rares variants « non O – non M » ont été classés dans le groupe N.
L'épuisement du système immunitaire
On a longtemps cru que le VIH (Lentivirus donc virus lent) cessait de se répliquer peu après l'infection, ce qui expliquait la phase de latence clinique de très longue durée, mais ne permettait pas de comprendre l’évolution secondaire défavorable de la maladie. En fait, le VIH engendre une infection chronique : il ne cesse pas de se reproduire
Dès la primo-infection, une multiplication intense du virus a lieu : chaque jour, un individu infecté produit cent millions (108) à un milliard (109) de virus tandis qu'en même temps plusieurs centaines de millions de lymphocytes Th sont détruits et remplacés !
Puis, dans les semaines qui suivent la primo-infection, on observe une diminution progressive du nombre de virus dans le sang, liée aux effets de la réponse immunitaire :
· les lymphocytes TCD8 cytotoxiques détruisent les lymphocytes Th infectés qui expriment les protéines virales
· les anticorps neutralisants empêchent l'infection des lymphocytes Th par les virions libérés.
Mais, bien qu'il paraisse "absent" dans le sang, le virus se réplique activement dans les tissus lymphoïdes (ganglions et rate). Les cellules dendritiques de ces tissus se comportent comme un réservoir de virus, et sont capables d'infecter en permanence les lymphocytes Th qui transitent ou y séjournent.
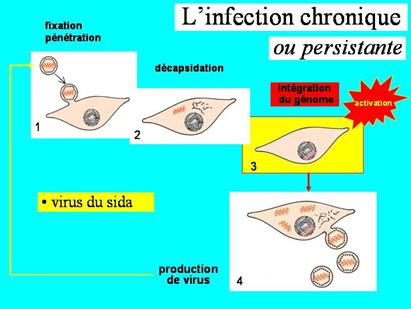
La latence clinique peut se caractériser par l’absence de signes cliniques en relation avec l’infection virale qui, elle, continuera à se manifester par une production virale chronique. La latence virale est une propriété bien connue des lentivirus qui se caractérise par l’extinction complète de toute transcription du provirus, mais, à partir de cette situation, le provirus intégré peut être réactivé. Des facteurs cellulaires et viraux assurent le subtil contrôle des cycles de latence/réactivation qui permettent alternativement au virus de s’exprimer et d’échapper à la réaction immunitaire, sachant qu’au cours de la latence, la cellule infectée n’extériorisera aucune protéine virale susceptible d’alerter le système immunitaire.
Tout au long de la latence clinique, des variants apparaissent. Certains variants échappent à la réponse immunitaire et prolifèrent. Le système immunitaire les reconnaît secondairement et réagit spécifiquement contre eux par de nouveaux lymphocytes Tc et de nouveaux anticorps.
Mais d'autres variants vont apparaître avec la possibilité d’échapper à la nouvelle réponse immunitaire. Le cycle se répète... Le VIH entraîne une infection chronique : l'éradication du virus est impossible.
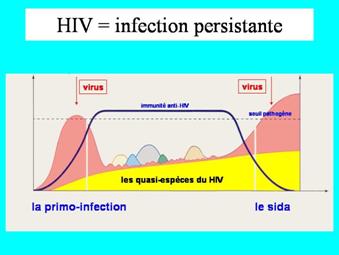
Chaque nouveau variant entraîne un certain niveau de destruction des lymphocytes Th, qui se raréfient progressivement.
Il serait possible de considérer qu’au bout de plusieurs années, les variations incessantes du VIH finissent par épuiser le système immunitaire : il s'en suivrait une réplication incontrôlée du virus et la disparition complète des lymphocytes Th. En fait, l’utilisation des antiviraux majeurs actuellement disponibles permet la plupart du temps de restaurer, tout au moins en partie, le nombre de Th circulants et les défenses immunitaires. La physiopathologie du Sida est donc beaucoup plus complexe. Elle met en jeu des facteurs viraux comme l’évolution des souches initiales vers le tropisme lymphocytaire, leur plus grande capacité réplicative et des facteurs d’ordre immunologique.
La longue période de latence clinique masque la lutte permanente entre le VIH et le système immunitaire.
IV – LA TRANSMISSION DU VIH
Le virus peut être isolé à partir de la plupart des liquides biologiques : sang, sperme, sécrétions vaginales, lait maternel, salive, larmes, LCR, urine, mais le VIH est un virus fragile qui ne peut donc se transmettre qu'à l'occasion de contacts interhumains "rapprochés".
|
|
Les voies de transmission des virus sont :
. la voie sexuelle . la voie sanguine . a transmission mère – enfant
|
|
avant tout sexuelle
La transmission sexuelle est le mode de contamination le plus fréquent. Elle peut s'effectuer au cours des rapports homosexuels ou hétérosexuels. Les premiers facteurs de risque sont les rapports non protégés et le "vagabondage" sexuel.
La porte d'entrée est la muqueuse génitale ou rectale. Les sécrétions génitales (sperme, glaire cervicale) sont infectantes par les virus libres mais surtout par les cellules infectées : lymphocytes TCD4 et macrophages.
· veineuse
- toxicomanie par voie IV
en Europe, à cause de la toxicomanie, la contamination par voie veineuse augmente et représente près de 40 % des cas d'infection par le VIH.
- transfusions sanguines
- accidents professionnels
avec des produits sanguins ou avec des objets contaminés (le risque de contamination à la suite d'une piqûre accidentelle est évalué à 0,4 %).
· materno-foetale
En l’absence de prophylaxie médicamenteuse, le taux de transmission du virus de la mère infectée à l'enfant est globalement évalué à 20 %. Il dépend avant tout du nombre de virus présents dans le sang maternel : plus ce nombre est élevé, plus le risque de transmission est grand.
Cette transmission peut se faire in utero dans les deux derniers mois (35 %) de la grossesse mais surtout au moment de l'accouchement (65 %).
La contamination par l'allaitement maternel est possible.
NB : 90 % des femmes VIH + vivent dans les pays en voie de développement.
En Ouganda, 15 % des femmes enceintes sont séropositives.
V - HISTOIRE DE LA MALADIE
Elle évolue en trois phases successives :
1° - la phase de primo-infection
Elle est symptomatique ou asymptomatique, c'est à dire cliniquement silencieuse.
La primo-infection symptomatique (chez 50 % des sujets infectés) se manifeste par des signes généraux peu spécifiques : adénopathies cervicales, fièvre, pharyngite avec dysphagie, fatigue, myalgies, courbatures, éruption maculopapuleuse. Ces symptômes ressemblent à ceux qu'on observe au cours de diverses affections virales aiguës (comme la mononucléose infectieuse), la primo-infection risque souvent de passer inaperçue.
Les premiers signes de primo-infection apparaissent en moyenne 20 jours après la contamination.
La primo-infection dure de 1 à 3 semaines. Cette phase correspond à
une multiplication virale intense et à la dissémination du virus
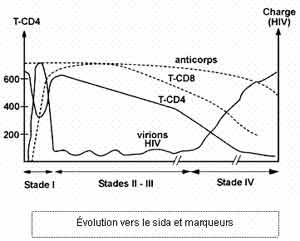
l'évolution vers le Sida est plus rapide après une primo-infection symptomatique qui s’accompagne d’une charge virale très élevée.
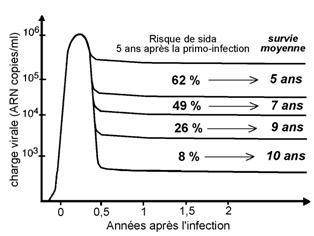
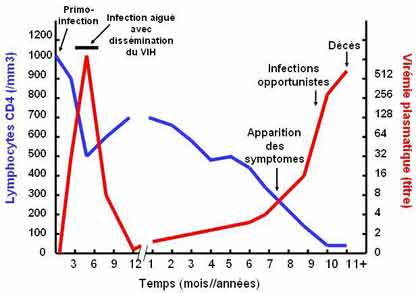
Évolution vers le sida et la mort après la primo-infection, en l'absence de traitement.
Le système immunitaire réagit à l'infection et, en quelques semaines, des anticorps apparaissent dans le sérum, dirigés contre l'ensemble des protéines du VIH, c'est la séroconversion : le sujet infecté devient séropositif.
2° - la phase asymptomatique
La deuxième phase est asymptomatique et peut être très prolongée (10 à 15 ans). Le virus se réplique continuellement dans les gîtes lymphoïdes : les lymphocytes TCD4 vont lentement, mais inexorablement, diminuer.
En dépit de la latence clinique, la période asymptomatique est le théâtre d'un équilibre entre la réplication virale, avec destruction des lymphocytes T CD4, et le renouvellement physiologique de ces lymphocytes : on estime que 10.9 particules virales sont produites chaque jour et que 10.9 lymphocytes T CD4 sont détruits et renouvelés dans le même temps.
3° - la phase clinique
La phase clinique correspond au Sida proprement dit :
lorsque le nombre de lymphocytes TCD4 devient inférieur à 200 / mm3 : le syndrome d'immunodéficience apparaît.
Les manifestations les plus fréquentes sont les infections opportunistes :
une infection opportuniste est une infection grave provoquée par un micro-organisme, habituellement non pathogène
- parce que contenu par le système immunitaire
- mais qui profite de l'opportunité offerte par l'immunodéficience.
Les principaux micro-organismes opportunistes sont :
|
des parasites |
Toxoplasme |
des bactéries |
Mycobacterium tuberculosis |
|
|
Cryptosporidium |
|
Mycobacterium avium |
|
|
Microsporidium |
|
Salmonella |
|
|
Leishmania |
|
|
|
des champignons |
Pneumocystis carinii |
des virus |
Herpes simplex (HSV) |
|
|
Cryptococcus neoformans |
|
Cytomegalovirus (CMV) |
|
|
Candida |
|
Virus varicelle-zona (VVZ) |
|
|
Histoplasma capsulatum |
|
|
L'immunodépression est également responsable de l'apparition de cancers :
· le sarcome de Kaposi : un virus de la famille des Herpesvirus, le HHV-8 (human herpesvirus 8), en est la cause ou le co-facteur.
· des lymphomes.
- les non-progresseurs à long terme
Dans la majorité des cas, les signes cliniques de déficit immunitaire apparaissent pendant les dix années suivant la séroconversion.
Néanmoins, un nombre restreint de sujets (5 à 10 %) demeurent cliniquement sains et immunologiquement normaux au-delà d'une décennie (jusqu'à 18 ans, à ce jour) : ce sont les sujets dits "non‑progresseurs à long terme".
Les critères retenus pour les non-progresseurs à long terme sont :
· une séropositivité depuis au moins huit ans
· un état clinique asymptomatique
· un taux de CD4 stables > à 500/ mm3
· pas de traitement antirétroviral
Chez ces sujets, la charge virale plasmatique est basse voire indétectable, mais elle persiste.
Ce groupe des sujets dits "non-progresseurs" est en fait hétérogène : certains sont véritablement "non-progresseurs au long cours" tandis que d'autres subissent une détérioration beaucoup plus lente de leur système immunitaire.
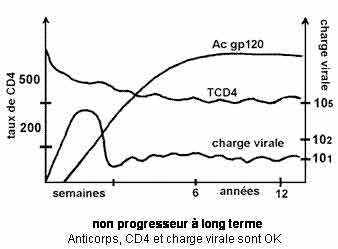
- la résistance à l'infection
On a remarqué dans des groupes de sujets à haut risque
- (homosexuels dont les partenaires étaient morts du Sida, hémophiles ayant reçu du sang contaminé)
- que quelques sujets n'étaient pas cliniquement atteints du Sida.
Beaucoup de ces sujets sont homozygotes pour une mutation portant sur le gène codant le co-récepteur CCR5 :
Le gène muté a subi une importante délétion. La protéine correspondante ne peut plus jouer son rôle de co‑récepteur pour l'entrée du VIH.
Cette mutation toucherait environ 1 % de la population de race blanche.
L'infection par le VIH entraîne une réponse immunitaire qui fait apparaître des anticorps dirigés contre toutes les protéines virales. La présence d'anticorps anti-VIH est le témoin de l'infection : un individu qui les possède est déclaré séropositif.
Le diagnostic sérologique s'opère en deux étapes :
1° : le test de dépistage : y a-t-il des anticorps anti-VIH ?
2° : la confirmation du test permet de préciser les différentes spécificités des anticorps vis à vis des différents antigènes viraux
Première étape : le test de dépistage
L'apparition des anticorps demande un certain temps…
Un certain temps s'écoule entre la contamination par le virus et l'apparition des anticorps. Pendant cette période, le sujet contaminé est infectieux mais la sérologie est négative.
Cette période est appelée la "fenêtre sérologique" : plus les techniques de détection s'améliorent, plus la fenêtre sérologique diminue : elle est actuellement de 22 jours en moyenne (avec des écarts de 6 à 38 jours).
Nous verrons que grâce à des tests combinés (ou mixtes), la détection associée de la p24 permet de raccourcir cette fenêtre. La détection des génomes viraux permet de la raccourcir, encore davantage.
Représentation des marqueurs virologiques au cours de la primo-infection par le VIH.
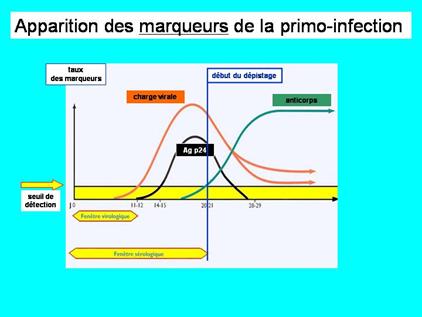
Le test de dépistage
Dans un dépistage, il est important d'éviter des résultats faussement négatifs : on utilise, pour cette raison, une technique sensible; La recherche des anticorps anti-VIH se fait à l'aide d'une technique ELISA (Enzyme-linked Immunosorbent assay) :
- des antigènes viraux (protéines d'enveloppe et de capside) sont fixés au fond d'une petite cupule.
- on ajoute le sérum à tester : s'il contient des anticorps spécifiques, ils sont "capturés" par les antigènes.
- on révèle la fixation des anticorps spécifiques du virus en ajoutant un anticorps anti-Ig humaine (de chèvre) auquel une enzyme a été accrochée (un "anti-anticorps" marqué).
- on ajoute le substrat de l'enzyme : l'hydrolyse du substrat par l'enzyme génère une coloration dont on apprécie l'intensité.
On pratique en même temps une réaction avec des sérums "témoins" positifs et négatifs.
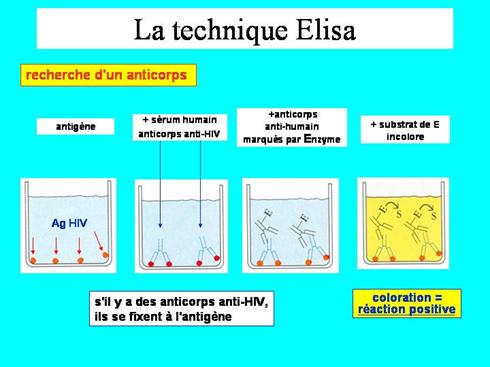

Deux tests différents sont pratiqués sur le même sérum et doivent permettre le dépistage des anticorps anti-VIH-1 et anti-VIH-2 :
- si la recherche est négative, on en reste là.
- si la recherche est positive, on passe à la 2ème étape
Deuxième étape : le test de confirmation
Pour confirmer un test, il est important d'éviter des résultats faussement positifs : on utilise pour cette raison, une technique spécifique.
Le test de confirmation vérifie que les anticorps détectés par le test de dépistage sont bien spécifiques du VIH. En effet, malgré sa spécificité supérieure à 99%, un test de dépistage peut parfois révéler, chez des sujets non-infectés, des anticorps qui "croisent" avec certains antigènes viraux..
1. le test de confirmation n'est pas pratiqué si les tests de dépistage sont négatifs.
2. tout dépistage positif, douteux ou discordant (un seul test positif sur les deux pratiqués) doit être confirmé.
|
|
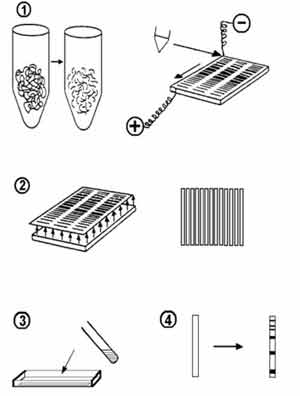
Le test de confirmation : le Western-blot
1- après fragmentation d'une culture de virus, les protéines virales sont séparées par électrophorèse en gel d’acrylamide dans lequel elles vont migrer en fonction de leur taille: les grosses molécules (gp 160, gp 120) migrant moins facilement que les petites (gp 41, p 17...). 2 - on transfère les protéines séparées en "buvardant" le gel (to blot = buvarder) avec une feuille de nitrocellulose. Cette feuille est découpée en bandelettes. 3 - on immerge une bandelette dans un petit bac contenant le sérum à contrôler : si ce sérum contient des anticorps spécifiques du VIH, ils se fixent aux antigènes. 4 - la fixation des anticorps est révélée par une technique ELISA identique à celle utilisée pour le test de dépistage : on ajoute un anticorps anti Ig humaines marqué par une enzyme puis le substrat de cette enzyme. Une bande colorée apparaît pour chaque protéine virale sur laquelle s'est fixée un anticorps.
|
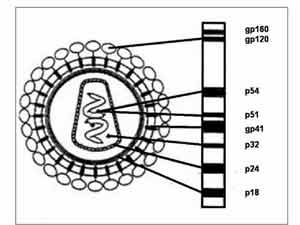
Critères de positivité du W-B définis par l'OMS
Le W-B doit révéler au moins deux bandes correspondant aux produits du gène env, (pour VIH-1 : les produits de ces gènes sont gp 160, gp 120, gp 41), et une bande correspondant à une protéine du gène gag, et ceci quelle que soit la réactivité d’autres bandes.
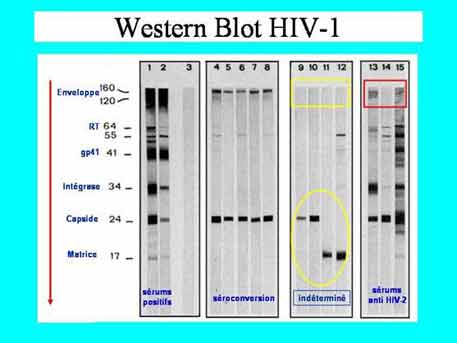
1° - chez un sujet séropositif, le Western-blot est "complet" : il met en évidence des anticorps dirigés contre l'ensemble des protéines virales. En cas de positivité du Western-blot, un deuxième prélèvement doit être dépisté pour affirmer la séroposivité.
2° - l'apparition de bandes colorées ne correspondant pas aux critères d'un W-B positif définit un W-B indéterminé. Ceci peut traduire :
· une séroconversion en cours pour le VIH-1 : elle sera affirmée par l'examen d'un nouveau sérum prélevé après un délai de 2 à 4 semaines au cours duquel les anticorps spécifiques vont atteindre un taux détectable et par une évaluation de la charge virale (quantification des génomes viraux circulants).
· une infection par le VIH-2 : qui devra être confirmée par un test spécifique de ce virus (ELISA et W-B).
· une réactivité non spécifique : si, sur un autre prélèvement pratiqué 2 à 4 semaines plus tard et a fortiori 2 à 3 mois plus tard, le profil du W-B reste identique, il s'agit d'une réactivité non-VIH : il n'y a pas d'infection par le VIH.
Autres tests pour le diagnostic biologique
· la recherche de l'antigène P 24
La protéine P 24 est la protéine majeure de la capside du VIH.
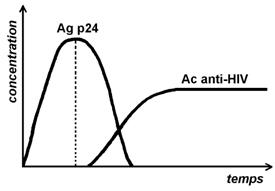
Dans le cas d'une personne présentant un syndrome de primo-infection symptomatique, la détection de l'antigène P 24 peut être intéressante car elle est positive pendant la phase sérologiquement muette.
L'antigénémie se négative dès la séroconversion : les anticorps anti-P 24 se fixent à l'antigène pour former des complexes immuns (Ag-Ac) qui sont éliminés.
|
|
|
p 24 apparaît dans le sang avant les anticorps anti-HIV |
L'antigène P 24 réapparaît au stade du Sida avéré, mais cet examen, autrefois considéré comme un marqueur de la réplication virale, est devenu à ce stade, inutile et déconseillé. Les techniques de quantification de la charge virale sont maintenant utilisées.
· les techniques de dépistage combiné
Elles sont capables de détecter simultanément les Ac anti-VIH-1/2 et l’Ag P24. Dans la période très précoce de séroconversion, ces techniques sont globalement plus sensibles que les simples techniques sérologiques classiques en réduisant la fenêtre sérologique de 2 à 5 jours. Elles peuvent constituer l’une des 2 techniques de dépistage et sont actuellement utilisées en routine comme tests de dépistage.
· l'isolement du virus en culture
L'isolement du virus est une technique longue et difficile, qui n'est pas utilisée en routine.
Elle était réservée au diagnostic de l'infection chez le nouveau-né de mère infectée, maintenant remplacée par les techniques de biologie moléculaire.
En effet, tous les nouveau-nés de mère séropositive sont séropositifs car les anticorps maternels ont franchi la barrière placentaire. Leur présence empêche le diagnostic sérologique de l'infection d'un nouveau-né.
La recherche s’effectue sur les cellules mononucléées du sang placées en coculture avec des cellules d’un donneur négatif en présence de phytohémagglutinine et d’IL2.
La présence du virus est détectée par la mise en évidence de l’Ag P 24 ou d’une activité transcriptase inverse dans le surnageant du milieu de culture.
· la détection du matériel génétique viral
On procède par amplification génique à l’aide de sondes spécifiques des séquences les plus conservées (gag et pol).
On peut rechercher, soit les séquences intégrées (l'ADN proviral cellulaire), soit l’ARN virionique après rétrotranscription (RT-PCR).
Cette technique remplace la culture du virus dans le diagnostic d'une infection à VIH chez le nouveau-né de mère infectée.
· l’appréciation de la résistance aux antiviraux dans le suivi des sujets infectés
Résistance phénotypique : par mesure en culture cellulaire (long et coûteux), uniquement utilisée dans certains protocoles.
Recherche de mutations associées à la résistance aux antiviraux : par amplification et séquençage des gènes pol (pour les inhibiteurs de RT et de protéase) et env (pour les inhibiteurs de fusion).
Examens de laboratoire accompagnant l’infection VIH
L'infection à VIH est une infection chronique dont les manifestations cliniques n'apparaissent qu'après une période plus ou moins prolongée, généralement plusieurs années.
Pour évaluer le pronostic de l'infection
on fait appel à l'interprétation de deux marqueurs biologiques:
1° - la numération sanguine des lymphocytes T CD4
2° - la mesure de la charge virale
1° - Évaluer l'atteinte du système immunitaire : les lymphocytes CD4
Le seul paramètre immunologique utile pour surveiller et prendre en charge les patients infectés par le VIH est le nombre absolu de lymphocytes CD4 circulants dans le sang.
Pour les distinguer des autres lymphocytes, on pratique un immuno-marquage avec des anticorps anti-CD4 fluorescents et on compte les cellules marquées par cytométrie de flux (une technique de numération automatique).
|
Valeurs normales des T CD4 : entre 600 et 1200/mm3 |
la numération des lymphocytes T CD4 est le paramètre irremplaçable du déficit immunitaire.
2° - Évaluer la réplication virale : la charge virale
La mesure de la concentration plasmatique de l'ARN du VIH (ou charge virale) évalue l'intensité de la réplication du virus dans l'organisme qui se situe en fait non pas dans le sang mais dans les organes lymphoïdes.
Le niveau de réplication du virus, évalué par la charge virale, est le paramètre le plus précis et le plus précoce pour prédire l'évolution clinique ultérieure.
Les déterminations successives de la charge virale permettent d’évaluer l’efficacité des traitements antirétroviraux.
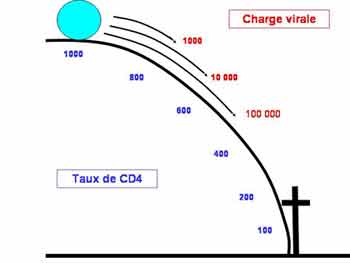
- le taux de lymphocytes T CD4 représente la distance qui sépare du bas de la pente
- la charge virale représente la vitesse
- la réponse immunitaire et le traitement antiviral sont les freins
Différentes techniques ont pu être proposées pour évaluer la charge virale :
1 - Amplification du signal d’hybridation
: (technique de l’ADN branché ou bDNA).
2 - Amplification de la cible :
- PCR quantitative : après rétrotranscription de l’ARN viral en ADN, polymérisation de l’ADN et quantification par comparaison avec un standard interne.
- NASBA : amplification isotherme de l’ARN
3- Les techniques de PCR en temps réél sont maintenant disponibles. Leur principe repose sur le suivi, cycle après cycle, du signal de détection de la cible amplifiée.
Compte tenu des variations de sensibilité des tests utilisés, il est important qu'un patient soit suivi dans un même laboratoire avec la même technique.
Les résultats sont présentés à la fois sous la forme de la charge virale proprement dite (nombre de molécules d'ARN viral ou copies par ml de sérum) et sous sa transformation logarithmique (log10 du nombre de copies / ml) :
Pourquoi en log ? :
- une baisse de la charge de 1 log est divisée par 10
- une baisse de la charge de 2 log est divisée par 100
On évite ainsi de mettre sur le même plan une charge virale qui passe de 500 000 à 400 000 et une charge virale qui chute de 100 000 à 10 000
|
charge virale plasmatique (copies/ml) |
charge virale plasmatique (log 10) |
|
200 |
log 10 (200) = 2,3 |
|
500 |
2,7 |
|
1000 |
3 |
|
5000 |
3,7 |
|
10 000 |
4 |
|
30 000 |
4,5 |
|
50 000 |
4,7 |
|
100 000 |
5 |
|
1 000 000 |
log 10 (1 000 000) = 6 |
L'incertitude sur la mesure de la charge virale est élevée.
On considère que seule une variation de 0,5 du log10 est significative : ce qui correspond à un nombre de copies multiplié ou divisé par 3. Ainsi :
· une charge virale qui passe de 10 000 à 50 000 copies / ml correspond à une réelle augmentation,
· alors que le fait de passer de 100 000 à 200 000 copies / ml n'est pas significatif.
La variabilité de la mesure est liée à deux phénomènes intriqués : l'un, technique, est la variabilité des conditions de mesure au laboratoire, l'autre est la fluctuation de la quantité de virus présents dans le plasma.
VII- SUIVI CLINIQUE ET BIOLOGIQUE D’UN PATIENT ATTEINT DE SIDA
|
examens recommandés |
bilan initial |
CD4 > 500 bilan tous les 6 mois |
CD4 entre 200 et 500 bilan tous les 3 mois |
|
Sérologie VIH (Western blot) |
+ |
|
|
|
NFS, plaquettes |
+ |
+ |
+ |
|
Lymphocytes CD4 |
+ |
+ |
+ |
|
Transaminases, g -GT |
+ |
|
|
|
Sérologies : syphilis, hépatite B, Hépatite C, toxoplasmose, CMV |
+ |
selon le résultat du bilan initial |
selon le résultat du bilan initial |
|
IDR à la tuberculine |
+ |
||
|
Radiographie du thorax |
+ |
||
|
Charge virale |
+ |
+ |
+ (–) |
| (–) la charge virale doit être réalisée 2 fois par an sauf en cas d'évolutivité et (ou) de mise en route d'un traitement antirétroviral. | |||
VIII - ELEMENTS DE THERAPEUTIQUE
Depuis la mise à disposition de la première molécule anti-VIH en 1986, (AZT = Rétrovir), la palette des antirétroviraux n'a cessé de s'élargir. Les molécules actuellement disponibles font partie de 3 familles :
- Les inhibiteurs nucléosidiques de la transcriptase inverse (INRT)
- Les inhibiteurs non-nucléosidiques de la transcriptase inverse (INNRT)
- Les inhibiteurs de la protéase (IP)
- Les inhibiteurs d’entrée du virus dans la cellule cible (inhibiteurs de fusion)
- En cours d’évaluation clinique, les inhibiteurs d’intégrase
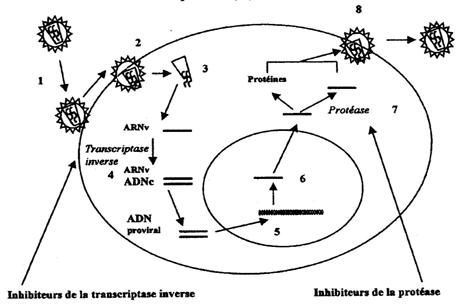
Les objectifs des traitements actuels sont de réduire la réplication virale le plus possible et le plus durablement possible en évitant la sélection de mutants résistants aux médicaments employés.
Pour ce faire, la stratégie actuelle associe en trithérapie 2 INRT + 1 IP ou 2 INRT + 1 INNRT
Indications :
c'est la numération des CD4 et la mesure de la charge virale qui guident le traitement :
- traitement des personnes symptomatiques et des personnes dont le nombre de CD4 est <350/mm3
- traitement indiqué aux personnes dont le nombre des CD4 est compris entre 350 et 500/mm3, mais peut être différé si la charge virale est stable et inférieure à 10000 copies/ml
- traitement de la primo-infection recommandé
IX - PREVENTION
Des mesures individuelles et collectives :
- dépistage systématique des donneurs de sang, la mise en oeuvre récente de la détection de l’ARN viral par RT-PCR, associée au dépistage des anticorps et de la p24, permet un dépistage plus précoce des éventuels flacons contaminés
- prévention de la transmission sexuelle par promotion de l'utilisation de préservatifs et par l'éducation et l'information
- lutte contre la toxicomanie et l'échange de seringues
- prévention de la transmission au personnel soignant : en cas d'accident d'exposition au sang (AES) provenant d'un patient infecté par le VIH, trithérapie pendant 4 semaines dès les premières heures.
Prévention de la transmission materno-foetale : traitement de la mère, poursuivi pendant l'accouchement et traitement de l'enfant pendant les 6 premières semaines de vie.
Deux situations :
- si la femme enceinte est déjà sous traitement pour elle-même, le traitement est poursuivi
- si la femme enceinte n’est pas traitée, un traitement est initié à la fin du 2ème trimestre de grossesse en l’absence de risque d’accouchement prématuré ou de charge virale élévée, ou dès le début du 2ème trimestre, en cas de risque d’accouchement prématuré ou si la charge virale est supérieure à 105 copies/ml.
Recherches vaccinales : les approches vaccinales traditionnelles ne sont pas envisageables
Pour des raisons de sécurité, impossibilité d'utiliser un rétrovirus atténué chez l'homme
La protection conférée par les vaccins inactivés se limite aux souches très proches de celle dont est issu le vaccin,
et devient rapidement inefficace du fait de la grande variabilité génétique et antigénique du virus.
SITUATION MONDIALE DU SIDA
Les statistiques suivantes sont extraites du site
http://www.pasteur.fr/actu/presse/documentation/onusida.html
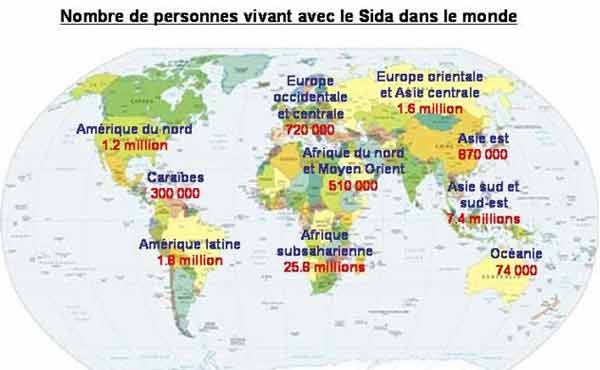
LE POINT SUR L'EPIDEMIE DE SIDA : DECEMBRE 2005 (ONUSIDA/OMS)
· Nombre de personnes vivant avec le VIH/SIDA dans le monde (carte) :40,3 millions (36,7-45,3 millions)
(38 millions d'adultes dont 17,5 millions de femmes et 2,3 millions d'enfants de moins de 15 ans) dont :
- 25,8 millions en Afrique subsaharienne (2,4 millions de décès en 2005)
- 7,4 millions en Asie du Sud et du Sud-Est (480 000 décès en 2005)
- 1,8 million en Amérique Latine (66 000 décès en 2005)
- 1,6 million en Europe orientale et Asie centrale (62 000 décès en 2005)
- 1,2 million en Amérique du Nord (18 000 décès en 2005)
- 870 000 en Asie de l'Est ( 41 000 décès en 2005)
- 720 000 en Europe occidentale et centrale (12 000 décès en 2005)
- 510 000 en Afrique du Nord et Moyen-Orient (58 000 décès en 2005)
- 300 000 dans les Caraïbes (24 000 décès en 2005)
- 74 000 en Océanie (3600 décès en 2005)
· Nombre de nouveaux cas d'infection à VIH en 2005 :
4,9 millions (4,3-6,6 millions)
(dont 4,2 millions d'adultes et 700 000 enfants de moins de 15 ans) dont :
- 3,2 millions en Afrique subsaharienne
- 990 000 en Asie du Sud et du Sud-Est
- 270 000 en Europe orientale et Asie centrale
- 200 000 en Amérique latine
- 140 000 en Asie de l'Est
- 67 000 en Afrique du Nord et Moyen-Orient
- 43 000 en Amérique du Nord
- 30 000 dans les Caraïbes
- 22 000 en Europe occidentale et centrale
- 82 00 en Océanie
· Nombre de décès dus au SIDA en 2005 :
3,1 millions (2,8-3,6 millions)
(dont 2,6 millions d'adultes et 570 000 enfants de moins de 15 ans) dont :
- 2,4 millions en Afrique subsaharienne
- 480 000 en Asie du Sud et du Sud-Est
- 66 000 en Amérique latine
- 62 000 en Europe orientale et Asie centrale
- 58 000 en Afrique du Nord et Moyen-Orient
- 41 000 en Asie de l'Est
- 24 000 dans les Caraïbes
- 18 000 en Amérique du Nord
- 12 000 en Europe occidentale et centrale
- 36 00 en Océanie
En 2003, 30 000 personnes vivaient avec le sida en France, où l'on estime à 100 000 le nombre de séropositifs, et où 6000 nouvelles contaminations sont recensées chaque année. Une personne sur deux avec un diagnostic de sida en 2004 ignorait sa séropositivité.
Pour en savoir plus : ONUSIDA

Cours proposé par le Pr Anne Decoster et le Dr Jean-Claude Lemahieu (Faculté Libre de Médecine de Lille)
Pour plus de précision, lire les chapitres et de « Virologie médicale » A. Mammette, Collection AZAY, Presses Universitaires de Lyon. 2002
Pour en savoir plus :
|
|
|
|
|