FRANCISELLA


Ces bactéries sont connues en France depuis 1946, date de la découverte de la maladie humaine dans ce pays. Elles étaient responsables d'un tableau clinique et épidémiologique particulier, évoqué en période de chasse, plus particulièrement chez les femmes de chasseurs ayant dépecé un lièvre.
Elles sont redevenues d'actualité, en particulier à cause de leur pouvoir pathogène important (agent biologique de la classe 3) susceptible d'être exploité lors d'une attaque bioterroriste (http://www.tdh.state.tx.us/bioterrorism/facts/tularemia.html, http://www.uhmc.sunysb.edu/microbiology/bioterrorism.htm).
Elles ont prouvé leur efficacité, en particulier lors de la seconde guerre mondiale, peu avant le siège de Stalingrad, en ralentissant l'avancée des divisions de panzers...........
2 - Historique
Découverte en 1911 par G.W. McCoy et C. W. Chapin en Californie dans le Comté de Tulare, la tularémie est primitivement une maladie mortelle (pseudo-peste) des animaux sauvages dont l'écureuil.
|
Elle pouvait affecter aussi le daim par l'intermédiaire d'un insecte piqueur (Deer fly fever ou fièvre de la mouche du daim). Découverte en France chez l'homme en 1946 (Doubs). Synonymes: Francis disease, rabbit fever, deer fly fever. |
 |
3 - Habitat
Il s'agit essentiellement d'une zoonose et on peut répartir les espèces animales dont les mammifères (190 connues) en trois groupes selon leur sensibilité, les espèces les plus réceptives étant les rongeurs (souris, cobayes) et les lagomorphes (lièvres).
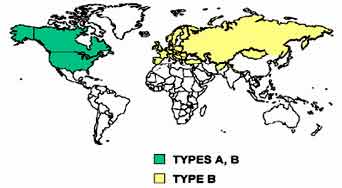
| La tularémie se rencontre principalement dans les zones boisées de l'hémisphère Nord: États-Unis d'Amérique, Europe du Nord avec la Suède, la Finlande……, la Russie et enfin le Japon. F. tularensis biovar tularensis (type A très virulent), est présente essentiellement aux États-Unis. F. tularensis biovar palearctica ou holarctica (type B, moins virulent) est présente en Europe et en Asie. http://bbrp.llnl.gov:80/bbrp/html D'autres espèces ou sous-espèces ont été exceptionnellement rapportées chez l'homme: F. philomiragia et F. tularensis biovar novicida et F. tularensis biovar mediasiatica (Asie). |
 |
4 - Epidémiologie
France
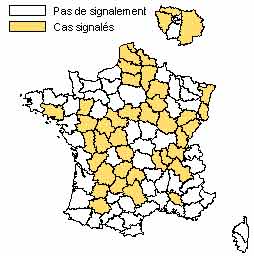
. Avoir la notion de lièvres infectés par département (taux de mortalité de l'ordre de 5%) selon l'enquête du réseau SAGIR de 1993-96)
(http://www.oncfs.gouv.fr/events/point_faune/suivi-sanitaire/tularemie.php).
| . Deux pics saisonniers sont habituellment décrits, surtout en hiver mais aussi en automme, mais peut sévir toute l'année.
. Les personnes exposées sont surtout les chasseurs ou leurs femmes appelées à dépecer ou à cuisiner ces animaux, les gardes-chasse, les gardes forestiers, les cultivateurs...(exposition professionnelle).
. Méfiez-vous lors de la préparation culinaire ou non d'un lièvre, de la présence d'une grosse rate (splénomégalie inconstante)(cf image ). . Diffusion : à travers la peau saine, au niveau des conjonctives, de l'oropharynx, ou des voies aériennes supérieures. . Apparait sous forme de cas isolés suite au dépeçage d'un lièvre ou bien à la suite d'un contact même bref avec un animal malade ou mort (mulot, campagnol....). . Des cas de tularémie sont maintenant rapportés après morsure de tique, griffade, morsure ou léchage par chat, voire chien ou encore après contact avec un rongeur (mulot, campagnol). |
 |
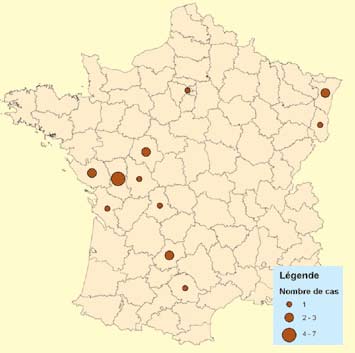
Le nombre de cas déclarés chez l'homme n'augmente pas en 2004 en France:
Europe :
. Europe Centrale et Ouest : lièvre d'Europe et tiques (Ixodes ricinus, Rhipicephalus sanguineus)
. Europe du Nord : lièvre variable, écureuils, lemmings et autres petits rongeurs.
Les moustiques sont aussi une source de contamination chez l'homme parmi d'autres vecteurs (taon.....).
Amérique du Nord:
. Etats-Unis, F. tularensis biogroupe tularensis est responsable de 70% des cas humains (mortalité 5 à 7%). Les tiques sont la principale source de l'infection en été. Les mammifères les plus atteints sont les lapins, les lièvres, les campagnols ou encore les moutons.
. Nord des Etats Unis - Canada : F. tularensis palearctica peut être trouvée et atteint les mammifères suivants : rat musqué, ou encore castor.
Ex-Union Soviétique : Les petits rongeurs sauvages et le lièvre constituent des sources de contamination directe de l'Homme en hiver. Les moustiques représentent la source dominante en automne.
Pour plus d'informations:
http://www.oie.int/fr/maladies/fr_mal.htm
5 - Pouvoir pathogène
En France, il s'agit essentiellement d'une maladie animale, en particulier du lièvre mais aussi des petits rongeurs tels mulot, campagnol........ Cette zoonose est donc transmise à l'homme par des léporidés infectés dont le lièvre (80% des observations). Maladie à déclaration obligatoire (à nouveau depuis 2002) elle est, cependant, reconnue comme maladie professionnelle dans le cadre du régime agricole (N°7)(gardes forestiers, bouchers, charcutiers, éleveurs, vétérinaires, ou encore technicien/ne).
En France, le nombre de cas annuel est faible: 18 à 72 cas entre 1987-1991. Il s’agit principalement de formes ulcéro-ganglionnaires par contact soit avec des rongeurs, soit le plus souvent avec des lièvres.
La transmission directe prédomine avec des voies de pénétration très variées:
- pénétration percutanée: F. tularensis est capable de franchir la peau saine mais pénètre de plus en plus chez l'homme, par piqûre d'arthropodes hématophages (moustique en Suède et tique aux Etats-Unis et le reste de l'Europe).
- pénétration par griffure, morsure, léchage.......
- pénétration conjonctivale: pénétration oculaire (frottement par main souillée, aérosol) ou oro-nasale (main souillée).
- pénétration orale: consommation de viande d'animaux infectés mais insuffisamment cuite, risque par l'eau contaminée.
- contamination par inhalation: aérosols produits dans les laboratoires lors d'autopsie de cadavres tel lièvre, de changement de litières etc... Les aérosols peuvent provenir de poussières de fourrage, de céréales, de laines souillées par excrétion de rongeurs. Cette forme sera privilégiée lors de bioterrorisme.
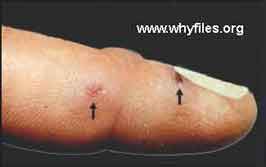
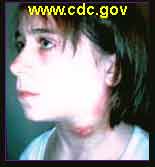
Les formes cliniques observées sont indiquées ci-dessous:

Exemples d'une forme cutanée et d'une forme ulcéro-ganglionnaire
6 - Physiopathologie
Outre le tropisme d'espèce très prononcé pour les rongeurs, les lagomorphes et accidentellement l'homme, il convient d'indiquer le tropisme d'organe avec l'atteinte du système réticulo-histiocytaire (rate, foie, noeuds lymphatiques) mais aussi le derme. Il s'agit de bactéries intracellulaires.
|
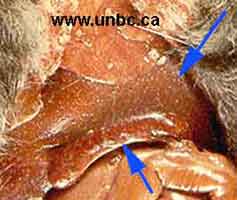
. Aprés pénétration (cutanée la plus courante ou d'une muqueuse), le germe se multiplie localement, et gagne les noeuds lymphatiques locaux pour passer finalement dans le sang. Puis il se multiplie dans le foie (multiple abcès visibles à l'oeil nu) et la rate (splénomégalie marquée)(cf image). Son nouveau passage dans le sang provoque une septicémie, souvent mortelle chez l'animal. |
 |
7 - Diagnostic biologique
Le diagnostic peut être difficile, d'autant qu'il est rare (18 cas en 1987, et 29 en 1991). Cependant le contexte épidémiologique est évocateur, donc à préciser au biologiste:
1/Toute l'année mais avec deux pics (automme et hiver) mais aussi en été après randonnée pédestre, promenade en forêt ou travaux des champs.
2/Patient consultant souvent pour une adénopathie douloureuse fistulisée d'un membre supérieur ou inférieur dans un contexte fébrile ou encore syndrome pseudogrippal.
3/Noter aussi la notion de chasse officielle et/ou de dépeçage de gibier.
4/Plus rarement, contact direct ou indirect avec un petit rongeur ou leurs excréta ou leurs parasites externes.........
5/ Piqûre par un insecte piqueur/suceur hématophage (tique, moustique.......)
Le diagnostic direct est presque impossible. Il s'agit le plus souvent d'une découverte fortuite suite à une culture de ponction ganglionnaire ou de sang (hémoculture).
|
ATTENTION AGENT DE LA CLASSE BIOLOGIQUE 3 |
 |
* Prélèvements à effectuer:
1/Sérosité au point d'inoculation (+++)
2/Ponction d'une adénopathie
3/Exsudats dans les formes conjonctivales ou pharyngées
4/Hémocultures devant un tableau de fièvre ou de septicémie
|
* Examen microscopique: Il est rarement positif à partir de la ponction ganglionnaire. Il peut s'agir d'une ou plusieurs hémocultures positives au deuxième ou troisième jour d'incubation en aérobiose. |
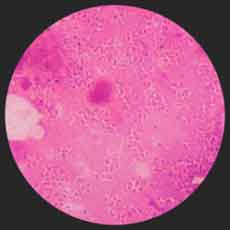 |
|
* Culture : Elle est lente (48 h à 5 jours au moins) et difficile à 37°C en aérobiose (Quelques souches poussent en présence de 5-7 % de CO2). Il convient d'utiliser des milieux enrichis tels la gélose chocolat enrichie (Polyvitex®), au sérum, glucosée, ou encore au jaune d'oeuf ou , flacons pour hémoculture, ou encore le milieu BCYE. La croissance est faible et lente (6 jours) sur la gélose au sang frais. |
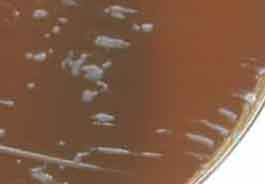 |
|
|
* Identification : d'abord présomptive basée sur la discordance de croissance en aérobiose entre une gélose nutritive (trypticase soja par exemple, à gauche) et une gélose chocolat supplémentée (à droite). |
|
Puis ENVOYER AU CNR - AFSSA (crée en octobre 2002). |
|
| * L'amplification génique (PCR) est possible mais encore peu utilisée directement sur produit pathologique (ganglion, par exemple) lors de diagnostic précoce et d'une très forte présumption compte tenu des commémoratifs et des éléments cliniques récoltés. Il est possible d'amplifier le gène codant pour la lipoprotéine de surface de 17 kDa (0,5 kb). - Cependant cette technique est très utile au diagnostic de genre, voire d'espèce après culture pour une identification plus rapide et plus sûre: Des amorces spécifiques du gène de l'ARNr 16S sont ainsi disponibles. Accessoirement le produit d'amplification de 1,1 kb est séquencé. |
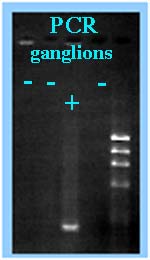 |
- Le diagnostic sérologique est la méthode la plus fréquemment positive faisant appel à la réaction classique d'agglutination en tube (cf ci-dessous) soit encore à une réaction d' immunofluorescence indirecte (IFI) ou ELISA. Ces réactions ont une spécificité médiocre, en particulier à la phase initiale:
|
* Précoce : positive au 10ème jour (> 1/40 ème) |
 |
|
Examens pouvant être effectués au CNR - Cahors |
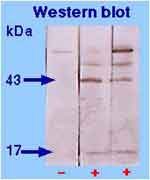 |
- La recherche d'une hypersensibilité retardée par l'intradermo-réaction à la tularine n'est plus utilisée, en l'absence d'antigène commercial.
- Inoculation expérimentale
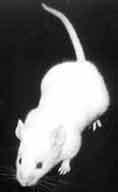
Compte tenu de la difficulté de diagnostic biochimique de cette bactérie, il est plus facile de tester la virulence de la souche isolée en inoculant une souris par voie IP ou SC, de préférence en Isolator® ou mieux disposer d'une animalerie protégée.
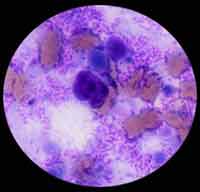
| La souris meurt de septicémie en 2 à 12 jours avec une adénopathie satellite et une splénomégalie (> 2 jours). Empreinte de la rate d'une souris infectée et morte à J6 par voie sous-cutanée après coloration de type MGG (à droite) |
 |
 |
NE PAS OUBLIER DE TRANSMETTRE LES DONNÉES
http://www.sante.gouv.fr/adm/dagpb/bo/2002/02-41/a0413306.htm
La surveillance épidémiologique repose sur la notification des cas, sur l'envoi de la souche isolée au CNR de la tularémie à l'AFSSA de Maisons-Alfort, pour identification du germe et typage des souches, et sur l'envoi du sérum au CNR de la tularémie au laboratoire de microbiologie du centre hospitalier de Cahors.
 Laboratoire d'études et de recherche en pathologie animale et zoonoses de l'AFSSA, unité des zoonoses bactériennes, 23, avenue Charles-de-Gaulle, B.P. 19, 94701 Maisons-Alfort Cedex, Dr Vaissaire (Josée), tél. : 01-49-77-13-00, courriel : j.vaissaire@afssa.fr, fax : 01-43-68-97-62 |
 Centre hospitalier, 335, rue du Président-Wilson, B.P. 269, 46005 Cahors, Dr Le Coustumier (Alain), tél. : 05-65-20-50-75, courriel : lecoustumier@ch-cahors.fr, fax : 05-65-20-51-10, |
* Cette bactérie est très sensible in vitro aux antibiotiques tels aminoglycosides (Streptomycine, Gentamicine), Tétracyclines, phénicolés et fluoroquinolones.
Le traitement classique s'appuiera sur les antibiotiques suivants: Streptomycine 30 mg/kg IM pendant 10-14 j ou Gentamicine 5 mg/kg/j IV x 10 j. L'alternative est Doxycycline 200 mg/j per os pendant 14-21 jours.
* Une association d'antibiotiques est recommandée à la phase précoce jusqu'à disparition de l'adénopathie.
* L'absence de résistance acquise et de standardisation de l'antibiogramme ne justifie pas sa mise en oeuvre
9 - Prophylaxie
Chez l'homme
Mesures générales: lutte contre les réservoirs et les vecteurs. Information des populations.
Prophylaxie sanitaire
. Emploi d'insecticides.
. Usage de vêtements de protection contre les arthropodes dans les zones d'enzootie (cf Borrelia).
. Emploi de masques, de gants et de lunettes pour manipuler et dépouiller les animaux sauvages.
. Désinfecter le pelage à l'eau de Javel avant autopsie.
. Ne pas boire d'eau non traitée en zone suspecte ou giboyeuse et bien cuire les viandes d'animaux sauvages en région d'enzootie.
. Respecter les règles générales d'hygiène.
|
Prophylaxie médicale: La fréquence de la maladie en France n'a pas justifié la mise en oeuvre d'un plan de vaccination comme dans d'autres pays tel USA. L'antibioprophylaxie sera à base de Doxycycline 100 mg q 12 h per os pendant 14 j, ou Tétracycline 500 mg po durant 14 j. |
 |
Chez l'animal
Prophylaxie sanitaire défensive: Agir sur le réservoir animal par le contrôle des densités de petits mammifères, lutter contre les arthropodes piqueurs, limitation des importations de lièvres d'Europe Centrale.
. Protection des élevages: quarantaine de déparasitage des nouveaux animaux, antibioprévention (streptomycine, tétracyclines) lors d'infection déclarée dans un élevage d'ovins ou de primates.
. Protection des locaux contre les rongeurs sauvages et séparation géographique, réelle, des espèces (pour éviter une contamination par des puces par exemple).
Prophylaxie sanitaire offensive: La tularémie n'est plus une maladie réputée légalement contagieuse chez toutes les espèces de rongeurs et de lagomorphes domestiques et sauvages. Leurs importations, morts ou vivants, ou celle de leur peau est soumise à contrôle.
Mesures de police sanitaire: Obligation de déclarer tout rongeur ou lagomorphe vivant ou mort suspect de tularémie ainsi que toute mortalité élevée de lièvres ou lapins de garenne.
. Si un cas est diagnostiqué, il faut une mise en interdit immédiate avec une visite sanitaire, un recensement et un abattage des animaux. Les cadavres sont aussi incinérés après autopsie.
. Pour les rongeurs et lagomorphes sauvages, une information est diffusée par l'ONC (http://www.oncfs.gouv.fr/) et le réseau SAGIR.
Ce cours a été préparé par le Professeur A. PHILIPPON (Faculté de Médecine COCHIN-PORT-ROYAL, Université PARIS V) et le Dr. J. VAISSAIRE (Responsable Secteur Bactériologie Spéciale à l'AFSSA de Maisons-Alfort - CNR Tularémie). Version du 08 02.05

http://www.sante.gouv.fr/adm/dagpb/bo/2002/02-41/a0413306.htm
http://www.invs.sante.fr/publications/guides_biotox/guide_tularemie.html
http://www.cnrs.fr/SDV/tularemie.html
http://www.oie.int/fr/normes/mcode/F_00111.htm
http://www.oie.int/fr/maladies/fr_mal.htm
http://www.oncfs.gouv.fr/events/point-faune/suivi-sanitaire/tularemie.htm
http://www.tularemie.org/
http://gsbs.utmb.edu/microbook/ch029.htm
http://www.tdh.state.tx.us/bioterrorism/facts/tularemia.html
http://www.uhmc.sunysb.edu/microbiology/bioterrorism.htm
|
|
|
|
|